
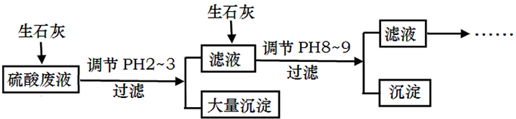
分析 硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl,
(1)硫酸的浓度为4.9g•L-1,结合c=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$计算;
(2)根据c(NH4+)越大,NH4+水解程度越小判断;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,并洗涤、干燥;
(5)①H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀;
②依据水解常数与电离常数及Kw的关系计算;
③根据还原剂还原性大于还原产物的还原性判断.
解答 解:硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl,
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=$\frac{\frac{4.9g}{98g/mol}}{1L}$=0.05mol/L,c(H+)=0.1mol/L,pH=-lg0.1=1,故答案为:1;
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)较大,因c(NH4+)越大,NH4+水解程度越小,则(NH4)2SO4溶液中c(NH4+)小于是NH4Cl溶液中c(NH4+)的2倍,如等于2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中$\frac{C(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$减小,故答案为:减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2开始沉淀;
②Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O?HAsO42-+OH-,该步水解的平衡常数Kh=$\frac{c(HAs{{O}_{4}}^{2-})c(O{H}^{-})}{c(As{{O}_{4}}^{3-})}$=$\frac{c(HAs{{O}_{4}}^{2-})c(O{H}^{-})}{c(As{{O}_{4}}^{3-})}$×$\frac{c({H}^{+})}{c({H}^{+})}$=$\frac{Kw}{{K}_{3}}$=$\frac{1{0}^{-14}}{4.0×1{0}^{-12}}$=2.5×10-3,
故答案为:2.5×10-3;
③已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.还原剂还原性大于还原产物的还原性,则还原性SO2>I->AsO33-,两个反应中还原性最强的微粒是SO2,
故答案为:SO2.
点评 本题考查较为综合,侧重于学生的分析、实验和计算能力的考查,明确沉淀溶解平衡的溶度积常数、水解常数和电离常数的计算及离子方程式的书写和沉淀的形成等是解本题关键,考查的知识点较多,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生的气体可在空气中燃烧 |
| (C)剧烈反应,产生可燃性气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生气体,可在空气中燃烧,溶液变成浅红色 |
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞的试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的有效成份是氯酸钙 | B. | 氟化氢溶于水形成的氢氟酸是强酸 | ||
| C. | 碘化钾水溶液能使淀粉变蓝 | D. | 氟气通入水中有氧气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com