
【题目】聚合硫酸铁简称聚铁[Fe2(OH)6-2n(SO4)n]m广泛用于饮用水等的净化。某化工厂利用硫酸铜废液制备聚铁,其流程如下:

回答下列问题:
(1)试剂A为__________。
(2)本实验中两次加入硫酸,其中“加热浓缩“时加入稀硫酸,除了抑制离子水解,还为了_______,“聚合”时加硫酸是为了控制溶液的pH在一定范围内,若pH偏大,则_________。
(3)“控温氧化”时选用绿色氧化剂双氧水,该过程需要控温的原因是________。
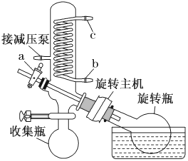
(4)减压蒸发装置如图所示。实验开始时,应先打开减压泵,从_____(填字母)口通入冷水,再打开旋转主机;实验结束时应先关闭旋转主机,再_______,打开阀门a通大气后,最后取下______(填仪器名称),从中获得聚铁。本实验采取减压蒸发的理由是___________。
(5)测定聚合硫酸铁样品主要成分的化学式。准确称取所得聚铁样品5.520g,溶于适量稀盐酸中,然后分成两等份:
a.一份加入过量的BaCl2溶液,然后过滤、洗涤、干燥,称重,得固体质量1.165g;
b.另一份置于250mL锥形瓶中,加入过量KI,充分反应后再用0.5000 molL-1Na2S2O3溶液滴定至终点,消耗标准溶液20.00mL。
已知:I2+2S2O32–=2I–+S4O62–(无色)
①计算所得产品化学式中n=_______。
②若m=4,写出“聚合”过程的化学方程式:______。
【答案】铁粉 增加H+浓度,提高双氧水的氧化能力(或促进Fe2+被氧化) Fe3+容易转化成Fe(OH)3沉淀,导致聚铁产率降低 温度过低反应速率慢,温度过高双氧水分解 b 关闭减压泵 旋转瓶 降低蒸发温度,防止加热时聚铁分解 1 4Fe2(SO4)3+16H2O=[Fe2(OH)4SO4]4+8H2SO4
【解析】
分析制备流程,利用硫酸铜废液制备聚铁,则将硫酸铜废液除酸后,需先加入一定量的铁粉,搅拌、过滤,得到硫酸亚铁溶液。向其中加入少量硫酸,一方面可在加热浓缩时抑制Fe2+的水解,另一方面为下一步氧化提供酸性环境,提高双氧水的氧化能力。通过双氧水将Fe2+氧化为Fe3+。该步骤注意控制反应温度。之后加入水和稀硫酸进行聚合,最后通过减压蒸发得到聚铁。据此分析解答。
(1)根据原料和产品可知将硫酸铜废液转化为聚铁,故硫酸铜废液除酸后,加入一定量铁粉,则可知试剂A为铁粉。答案为:铁粉;
(2)由分析可知,加入少量稀硫酸,除了在加热浓缩时抑制Fe2+的水解,还为下一步氧化提供酸性环境,提高双氧水的氧化能力。“聚合”时加硫酸是为了控制溶液的pH在一定范围内,若pH偏小时,Fe3+水解程度弱,pH偏大时,Fe3+容易转化成Fe(OH)3沉淀,导致聚铁产率降低;答案为:增加H+浓度,提高双氧水的氧化能力(或促进Fe2+被氧化);Fe3+容易转化成Fe(OH)3沉淀,导致聚铁产率降低;
(3)控制温度在一定范围内,一方面是为了加快反应速率,另一方面是防止双氧水分解,答案为:温度过低反应速率慢,温度过高双氧水分解;
(4)该装置使用减压泵给系统减压,降低溶液的沸点,可以在较低温度下蒸馏,避免产品聚铁分解。实验开始时,先打开减压泵使系统处于负压状态,再从用于冷凝蒸出物的(蛇形)冷凝管下口即b口通入冷水,从上口即c口排出;要将聚铁与水分离,因为水的沸点相对聚铁要低,故水浴锅温度调至减压条件下水的沸点附近,打开电动机转动旋转瓶,旋转瓶置于水浴中一边旋转,一边加热,可以增大蒸发面积,利于瓶内溶液扩散蒸发。结束时应先停止旋转电动机,防止蒸馏烧瓶在转动中脱落,再打开通气阀通大气,然后取下收集瓶和旋转瓶。实验中通过水浴加热是蒸发溶剂水,故水在收集瓶中,聚铁在旋转瓶中,取下旋转瓶得聚铁。答案为:b;关闭减压泵;旋转瓶;降低蒸发温度,防止加热时聚铁分解;
(5)①n(SO42-)=n(BaSO4)=![]() ,依据关系式:2Fe3+~I2~2S2O32-,可知n(Fe3+)=n(S2O32-)=
,依据关系式:2Fe3+~I2~2S2O32-,可知n(Fe3+)=n(S2O32-)=![]() ,
,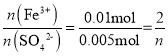 ,n=1。答案为:1;
,n=1。答案为:1;
②若m=4,说明Fe2(SO4)3“聚合”生成[Fe2(OH)4SO4]4,即部分Fe3+水解,反应方程式为:4Fe2(SO4)3+16H2O=[Fe2(OH)4SO4]4+8H2SO4。答案为:4Fe2(SO4)3+16H2O=[Fe2(OH)4SO4]4+8H2SO4。


 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
【题目】25℃时,醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+ H+,下列说法正确的是
CH3COO-+ H+,下列说法正确的是
A.向体系中加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单二苯乙炔类化合物是![]() 。以互为同系物的芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
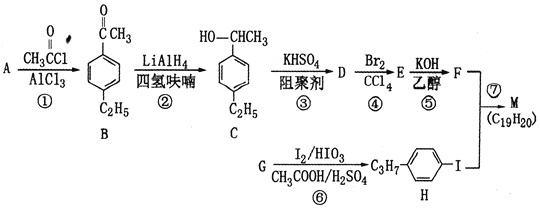
回答下列问题:
(1)G的结构简式为________________。
(2)C中含有的官能团名称是________________________。
(3)反应②的反应类型是________________,反应⑥的反应类型是________________。
(4)反应⑤的化学方程式为____________________。
(5)能同时满足下列条件的B的同分异构体有________种(不考虑立体异构)。
①苯环上有两个取代基 ②能发生银镜反应
写出其中核磁共振氢谱为5组峰,且峰面积之比为6:2:2:1:1的同分异构体的结构简式_______。
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线。_________________________
的合成路线。_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 取一定量固体溶解,向溶液中通入足量的CO,观察到有晶体析出 | 原固体中一定含Na2CO3 |
B | 取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成 | 原固体中一定含有Na2CO3 |
C | 取一定量固体,溶解,向溶液中滴加适量AgNO3 溶液,观察有白色沉淀生成 | 原固体中一定含有NaCl |
D | 称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分反应后,收集到有0.88g气体 | 原固体中三种物质都有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~L分别表示中学化学中常见的一种物质,其中A、G为常见的金属单质,K、L为气体,K能使湿润的红色石蕊试纸变蓝,M由两种元素组成,其质量比8:1。
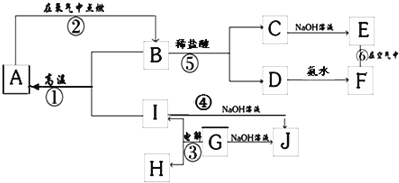
(1)K的电子式为_____
(2)反应②的离子方程式:_____,反应③的离子方程式:_____
(3)反应④的化学方程式:_____,反应⑥的化学方程式_____
(4)已知A和K反应为置换反应,则M的化学式为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应A+B![]() mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,问:
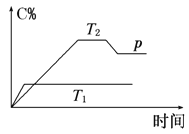
(1)温度T1________T2(填“大于”“等于”或“小于”)。
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2(填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强________(填“增大”“减小”或“不变”),平衡___ _____移动(填“向正反应方向”“向逆反应方向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的![]() 元素的基态原子核外电子排布式:____________________。
元素的基态原子核外电子排布式:____________________。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是______________________。
(3)![]() 分子中中心原子的杂化轨道类型是_________________,
分子中中心原子的杂化轨道类型是_________________,![]() 微粒的空间构型是_____________。
微粒的空间构型是_____________。
(4)![]() 被认为是有机化学中的“万能还原剂”,
被认为是有机化学中的“万能还原剂”,![]() 的电子式为_____________,其中三种元素的电负性由大到小的顺序是_____________________。
的电子式为_____________,其中三种元素的电负性由大到小的顺序是_____________________。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作![]() ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个![]() 和两个
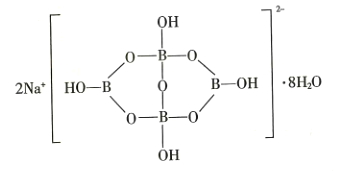
和两个![]() 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成![]() ,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是_______________(填字母)。
,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是_______________(填字母)。
A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力

(6)磷化硼的晶胞如图所示,其化学式为____________,若晶胞中硼原子与磷原子之间的最近核间距为apm,则晶胞边长为____________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学设计实验实现几种价态硫元素的转化。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红
(1)写出实现转化的化学方程式_______________
(2)设计实验,证明实现了该转化(写出操作和现象)_______________。
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
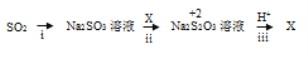
(3)i中加入的物质是__________ ,该转化利用的是SO2的_______性质。
(4)写出iii的离子方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ag 硝酸钾溶于bg水,形成VmL饱和溶液。下列关系式错误的是( )
A. 该溶液的物质的量浓度:c(KNO3)=![]() mol·L-1
mol·L-1
B. 该溶液的质量分数:w(KNO3)=![]() %
%
C. 20 ℃时KNO3的溶解度S=![]() g
g
D. 该溶液的密度ρ=![]() g·L-1
g·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com