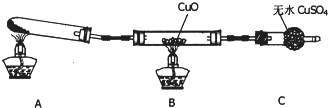
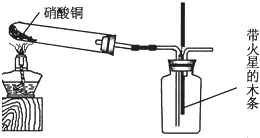
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用.回答下列问题:
(1)氮元素原子的L层电子数为
5
5
;
(2)NH
3与NaClO反应可得到肼(N
2H
4),该反应的化学方程式为
2NH3+NaClO=N2H4+NaCl+H2O
2NH3+NaClO=N2H4+NaCl+H2O
;
(3)肼可作为火箭发动机的燃料,与氧化剂N
2O
4反应生成N
2和水蒸气.
已知:
①N
2(g)+2O
2(g)=N
2O
4(l)△H
1=-19.5kJ?mol
-1②N
2H
4(l)+O
2 (g)=N
2(g)+2H
2O(g)△H
2=-534.2kJ?mol
-1写出肼和N
2O
4反应的热化学方程式
2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9KJ/mol
2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9KJ/mol
;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
N2H4+4OH--4e-=4H2O+N2↑
N2H4+4OH--4e-=4H2O+N2↑
.
Ⅱ、一定质量的液态化合物XY
2,在标准状况下的一定质量的O
2中恰好完全燃烧,反应方程式为:XY
2(l)+3O
2(g)═XO
2(g)+2YO
2(g),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g?L
-1,则:
(1)反应前O
2的体积是
672ml
672ml
.
(2)化合物XY
2的摩尔质量是
76g/mol
76g/mol
.
(3)若XY
2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为
C
C
和
S
S
(写元素符号).