
| A. | ②⑥⑦⑧ | B. | ③④⑤⑥ | C. | ③④⑥⑦ | D. | ①②⑧ |
分析 可以从以下方面判断醋酸是否是弱电解质:电离平衡方面、水解方面、离子浓度方面,据此判断正误.
解答 解:①醋酸与水能以任意比互溶,不能说明醋酸的电离程度,所以不能证明醋酸是弱酸,故错误;
②醋酸溶液能导电,只能说明醋酸能电离,不能说明醋酸的电离程度,所以不能证明醋酸是弱酸,故错误;
③醋酸稀溶液中存在醋酸分子,说明醋酸存在电离平衡,能证明醋酸是弱酸,故正确;
④常温下,0.1mol/L醋酸的pH比0.1mol/L盐酸的pH大,说明醋酸不完全电离,能证明醋酸是弱酸,故正确;
⑤醋酸能和碳酸钙反应放出CO2,说明醋酸酸性比碳酸强,但不能说明醋酸的电离程度,所以不能证明醋酸是弱酸,故错误;
⑥0.1mol/L醋酸钠溶液pH=8.9,其水溶液呈碱性,说明醋酸是强碱弱酸盐,所以能说明醋酸是弱酸,故正确;
⑦大小相同的铁片与同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢,说明醋酸中氢离子浓度小于盐酸中氢离子浓度,则证明醋酸是弱酸,故正确;
⑧0.1mol•L-1醋酸溶液能使紫色石蕊试液变红,说明醋酸溶液显酸性,醋酸发生了电离,但是不能说明醋酸的电离程度,所以不能证明醋酸是弱酸,故错误.
故选C.
点评 本题考查弱电解质的判断方法,明确弱电解质在水中电离不完全是解答本题的关键,学生应注意在平时的学习中归纳判断弱电解质的方法,难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | MgCl2(熔融) $\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ | B. | Al2O3+3C $\frac{\underline{\;2125℃\;}}{\;}$2Al+3CO↑ | ||
| C. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | HgS+O2$\frac{\underline{\;焙烧\;}}{\;}$ Hg+SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCH4和CH3Cl的混合物所含有的分子数目为NA | |
| B. | 1mol过氧化氢分子中共用电子对数为3NA | |
| C. | 用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 | |
| D. | 0.1mol Na2CO3•10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
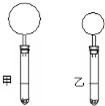 右下图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙完全反应后,所观察到的实验现象(反应过程中产生的气体全部收集在试管上部的气球中).下列说法不正确的是( )
右下图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙完全反应后,所观察到的实验现象(反应过程中产生的气体全部收集在试管上部的气球中).下列说法不正确的是( )| A. | 乙试管中盛放的是盐酸溶液 | |
| B. | 甲试管中盛放的是醋酸溶液 | |
| C. | 反应开始时的速率:甲>乙 | |
| D. | 反应结束时消耗碳酸钙的质量:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含等物质的量的AlO2-、OH-、SO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、SO32- | |
| B. | 在含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中缓慢通入SO2:KOH、Ba(OH)2、BaSO3 | |
| D. | 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入锌粉:Ag+、Cu2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
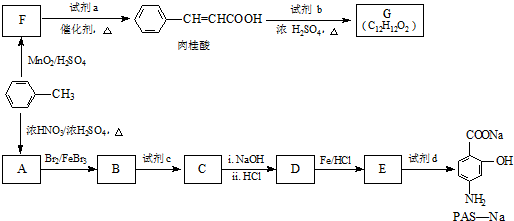
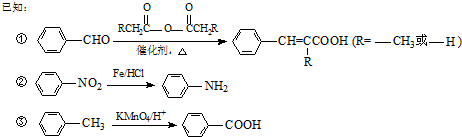
 生成A的反应类型是取代反应.
生成A的反应类型是取代反应.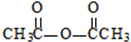 .
.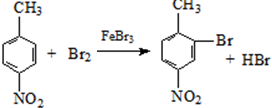 .
.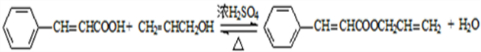 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | K闭合时,c电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B. | 当电路中转移0.4mol电子时,I中消耗的H2SO4为0.2 mol | |
| C. | K闭合时,II中SO42-向c电极迁移 | |
| D. | K闭合一段时间后,II可单独作为电源,d电极为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com