
·ÖĪö ŌŚ±„ŗĶĀČ»ÆÄĘČÜŅŗÖŠĶØČė°±ĘųŗĶ¶žŃõ»ÆĢ¼æɵƵ½Ģ¼ĖįĒāÄĘ³ĮµķŗĶĀČ»Æļ§ČÜŅŗ£¬¹żĀĖµĆ³ĮµķĪļĪŖĢ¼ĖįĒāÄĘ£¬¾Ļ“µÓ”¢øÉŌļµĆĢ¼ĖįĒāÄĘ¹ĢĢ壬ĀĖŅŗÖŠÖ÷ŅŖČÜÖŹĪŖĀČ»Æļ§£¬ŌŁ¼ÓČėĀČ»ÆÄĘŗĶĶØČė°±Ęų£¬½«ČÜŅŗ½µĪĀ½į¾§æɵĆĀČ»Æļ§¾§Ģ壬
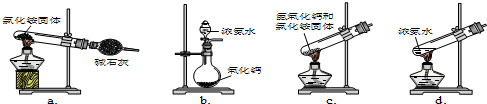
£Ø1£©ŹµŃéŹŅÖĘ°±ĘųæÉŅŌÓĆĀČ»Æļ§¹ĢĢåŗĶĒāŃõ»ÆøĘ¼ÓČČ£¬Ņ²æÉŅŌÓĆÅØ°±Ė®¼ÓČČ£¬¾Ż“ĖŃ”Ōń×°ÖĆ£»
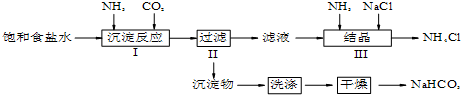
£Ø2£©²½ÖčIÖŠĀČ»ÆÄĘ”¢Ė®”¢°±ĘųŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ”¢ĀČ»Æļ§£¬ÓÉÓŚ°±ĘųŌŚĖ®ÖŠČܽā¶Č½Ļ“ó£¬ĖłŅŌĻČĶØ°±Ęų£¬°±ĘųŅ×ČÜÓŚĖ®£¬ĖłŅŌŅŖ×¢Ņā·ĄÖ¹µ¹Īü£»
£Ø3£©²½ÖčIIIŹĒĻņĀČ»Æļ§ČÜŅŗÖŠĶØČė°±Ęų£¬æÉŅŌŌö“óNH4+µÄÅØ¶Č£¬Ź¹NH4Cløü¶ąµŲĪö³ö£¬Ķ¬Ź±Ź¹NaHCO3×Ŗ»ÆĪŖNa2CO3£¬ĢįøßĪö³öµÄNH4Cl“æ¶Č£¬ÓÉÓŚĀČ»Æļ§µÄČܽā¶ČŹÜĪĀ¶ČÓ°Ļģ½Ļ“ó£¬ĖłŅŌŅŖ“ÓĀČ»Æļ§ČÜŅŗÖŠ»ńµĆĀČ»Æļ§¹ĢĢåæÉŅŌÓĆ½µĪĀ½į¾§µÄ·½·Ø£¬ĀČ»Æļ§ŹÜČČ·Ö½āÉś³É°±Ęų£¬æÉŅŌÓĆŹŖČóŗģÉ«ŹÆČļŹŌÖ½¼ģŃ飻
£Ø4£©ŹµŃéÖŠ²ā¶ØNaHCO3ŗ¬Į棬æÉŅŌ½«NaHCO3ČܽāŌŚĖ®ÖŠµĆµ½ČÜŅŗ£¬ŌŚČÜŅŗÖŠ¼ÓČė×ćĮæµÄĒāŃõ»Æ±µČÜŅŗ£¬øł¾Ż²śÉśĢ¼Ėį±µµÄÖŹĮææÉČ·¶Øѳʷ֊Ģ¼ĖįĒāÄʵÄÖŹĮ棬½ų¶ų¼ĘĖć³öĢ¼ĖįĒāÄʵÄÖŹĮæ·ÖŹż£¬ĪŖĮĖ×¼Č·³ĘĮæĖłµĆĢ¼Ėį±µ³ĮµķµÄÖŹĮ棬¶Ō³ĮµķŌŚ¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ£¬ĄäČ“”¢³ĘĮæŗóŅŖ½ųŠŠŗćÖŲ²Ł×÷£¬¾Ż“Ė“šĢā£»
½ā“š ½ā£ŗŌŚ±„ŗĶĀČ»ÆÄĘČÜŅŗÖŠĶØČė°±ĘųŗĶ¶žŃõ»ÆĢ¼æɵƵ½Ģ¼ĖįĒāÄĘ³ĮµķŗĶĀČ»Æļ§ČÜŅŗ£¬¹żĀĖµĆ³ĮµķĪļĪŖĢ¼ĖįĒāÄĘ£¬¾Ļ“µÓ”¢øÉŌļµĆĢ¼ĖįĒāÄĘ¹ĢĢ壬ĀĖŅŗÖŠÖ÷ŅŖČÜÖŹĪŖĀČ»Æļ§£¬ŌŁ¼ÓČėĀČ»ÆÄĘŗĶĶØČė°±Ęų£¬½«ČÜŅŗ½µĪĀ½į¾§æɵĆĀČ»Æļ§¾§Ģ壬
£Ø1£©ŹµŃéŹŅÖĘ°±ĘųæÉŅŌÓĆĀČ»Æļ§¹ĢĢåŗĶĒāŃõ»ÆøĘ¼ÓČČ£¬ÓĆ¹Ģ”¢¹Ģ¼ÓČȵÄ×°ÖĆ£¬Ņ²æÉŅŌÓĆÅØ°±Ė®¼ÓČČ£¬ÓĆŅŗĢå¼ÓČȵÄ×°ÖĆ£¬¹ŹŃ”b”¢d£»
£Ø2£©²½ÖčIÖŠĀČ»ÆÄĘ”¢Ė®”¢°±ĘųŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ”¢ĀČ»Æļ§£¬·“Ó¦·½³ĢŹ½ĪŖNaCl+NH3+CO2+H2O=NaHCO3”ż+NH4Cl£¬ÓÉÓŚ°±ĘųŌŚĖ®ÖŠČܽā¶Č½Ļ“ó£¬ĖłŅŌĻČĶØ°±Ęų£¬°±ĘųŅ×ČÜÓŚĖ®£¬ĖłŅŌŅŖ×¢Ņā·ĄÖ¹µ¹Īü£¬ĖłŅŌ“Ób¹ÜĶØČė£¬
¹Ź“š°øĪŖ£ŗNaCl+NH3+CO2+H2O=NaHCO3”ż+NH4Cl£»b£»°±Ęų£»
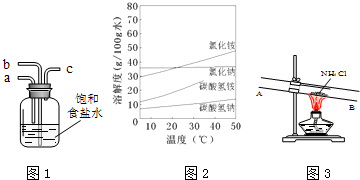
£Ø3£©²½ÖčIIIŹĒĻņĀČ»Æļ§ČÜŅŗÖŠĶØČė°±Ęų£¬æÉŅŌŌö“óNH4+µÄÅØ¶Č£¬Ź¹NH4Cløü¶ąµŲĪö³ö£¬Ķ¬Ź±Ź¹NaHCO3×Ŗ»ÆĪŖNa2CO3£¬ĢįøßĪö³öµÄNH4Cl“æ¶Č£¬ÓÉÓŚĀČ»Æļ§µÄČܽā¶ČŹÜĪĀ¶ČÓ°Ļģ½Ļ“ó£¬ĖłŅŌŅŖ“ÓĀČ»Æļ§ČÜŅŗÖŠ»ńµĆĀČ»Æļ§¹ĢĢåæÉŅŌÓĆ½µĪĀ½į¾§µÄ·½·Ø£¬ĀČ»Æļ§ŹÜČČ·Ö½āÉś³É°±Ęų£¬æÉŅŌÓĆŹŖČóŗģÉ«ŹÆČļŹŌÖ½¼ģŃ飬
¢Łøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬ĶØČė°±ĘųµÄ×÷ÓĆŹĒŌö“óNH4+µÄÅØ¶Č£¬Ź¹NH4Cløü¶ąµŲĪö³ö”¢Ź¹NaHCO3×Ŗ»ÆĪŖNa2CO3£¬ĢįøßĪö³öµÄNH4Cl“æ¶Č£¬¹ŹŃ”ac£»
¢ŚÓÉÓŚĀČ»Æļ§µÄČܽā¶ČŹÜĪĀ¶ČÓ°Ļģ½Ļ“ó£¬ĖłŅŌŅŖ“ÓĀČ»Æļ§ČÜŅŗÖŠ»ńµĆĀČ»Æļ§¹ĢĢåæÉŅŌÓĆ½µĪĀ½į¾§µÄ·½·Ø£¬
¹Ź“š°øĪŖ£ŗ½µĪĀ½į¾§£»
¢Ūøł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬ŃéÖ¤ĖłµĆµÄ¾§ĢåÖŠŗ¬ÓŠNH4+µÄ¾ßĢå²Ł×÷ŹĒȔɣĮ澧ĢåÓŚÓ²ÖŹŹŌ¹Ü£¬¶Ō¾§Ģå²æĪ»¼ÓČČ£®²¢ŌŚA “¦·ÅÖĆŹŖČóŗģÉ«ŹÆČļŹŌÖ½ŹŌÖ½£¬¹Ū²ģĻÖĻó£¬
¹Ź“š°øĪŖ£ŗA£»ŹŖČóŗģÉ«ŹÆČļŹŌÖ½£»
£Ø4£©ŹµŃéÖŠ²ā¶ØNaHCO3ŗ¬Į棬æÉŅŌ½«NaHCO3ČܽāŌŚĖ®ÖŠµĆµ½ČÜŅŗ£¬ŌŚČÜŅŗÖŠ¼ÓČė×ćĮæµÄĒāŃõ»Æ±µČÜŅŗ£¬øł¾Ż²śÉśĢ¼Ėį±µµÄÖŹĮææÉČ·¶Øѳʷ֊Ģ¼ĖįĒāÄʵÄÖŹĮ棬½ų¶ų¼ĘĖć³öĢ¼ĖįĒāÄʵÄÖŹĮæ·ÖŹż£¬ĪŖĮĖ×¼Č·³ĘĮæĖłµĆĢ¼Ėį±µ³ĮµķµÄÖŹĮ棬¶Ō³ĮµķŌŚ¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ£¬ĄäČ“”¢³ĘĮæŗóŅŖ½ųŠŠŗćÖŲ²Ł×÷£¬
¢Łøł¾ŻÉĻĆęµÄŹµŃé²½ÖčæÉÖŖ£¬½«×¼Č·³ĘĮæѳʷČÜÓŚĖ®£¬¼ÓČė×ćĮæBa£ØOH£©2ČÜŅŗ£¬
¹Ź“š°øĪŖ£ŗ×¼Č·³ĘĮæѳʷ£»¼ÓČė×ćĮæBa£ØOH£©2ČÜŅŗ£»
¢Ś¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ£¬ĄäČ“”¢³ĘĮ棬²¢½ųŠŠŗćÖŲ²Ł×÷£¬
¹Ź“š°øĪŖ£ŗŗćÖŲ£»
¢ŪČōŹż¾Ż“¦ĄķŹ±½«ĖłµĆ¹ĢĢåÖŹĮæ1.977g“ķæ“ĪŖ1.971g£¬ŌņÓÉ“Ė²śÉśµÄĻą¶ŌĪó²īĪŖ$\frac{1.971g-1.977g}{1.977g}$”Į100%=-0.3%£¬
¹Ź“š°øĪŖ£ŗ-0.3%£®
µćĘĄ ±¾ĢāŹĒĄūÓĆŗīŹĻÖĘ¼ī·ØµÄŌĄķæ¼²éĮĖŹµŃ黳±¾²Ł×÷ŗĶŹµŃéŌĄķ·ÖĪö£¬ÄŃ¶Č²»“󣬓šĢāŹ±ŅŖ×¢Ņā¶ŌŹµŃéŌĄķµÄĄķ½āÓėÓ¦ÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=-483.6 kJ•mol-1ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ•mol-1 | |
| B£® | ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0””Ōņ½šøÕŹÆ±ČŹÆÄ«µÄ¼üÄÜ“ó | |
| C£® | ŅŃÖŖNaOH£Øag£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H=-57.4 kJ•mol-1Ōņŗ¬20.0g NaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7kJµÄČČĮæ | |
| D£® | ŅŃÖŖ2C£Øs£©+2O2£Øg£©=2CO2£Øg£©”÷H1 2C£Øs£©+O2£Øg£©=2CO£Øg£©”÷H2£¬Ōņ”÷H1£¾”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® | 26M3+ | C£® | 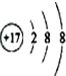 | D£® | 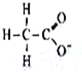 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
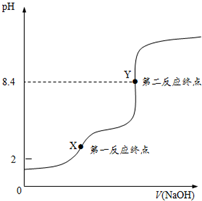 H2C2O4•2H2O£Ø²ŻĖį£¬¶žŌŖČõĖį£©ŗĶĮŚ±½¶ž¼×ĖįĒā¼Ų¾łæÉ×÷ĪŖ±ź¶ØNaOHČÜŅŗÅØ¶ČµÄ»ł×¼ĪļÖŹ£¬“Ó¶ų»ńµĆNaOH±ź×¼ČÜŅŗ£®
H2C2O4•2H2O£Ø²ŻĖį£¬¶žŌŖČõĖį£©ŗĶĮŚ±½¶ž¼×ĖįĒā¼Ų¾łæÉ×÷ĪŖ±ź¶ØNaOHČÜŅŗÅØ¶ČµÄ»ł×¼ĪļÖŹ£¬“Ó¶ų»ńµĆNaOH±ź×¼ČÜŅŗ£®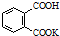 £¬Ä¦¶ūÖŹĮæĪŖ204g•mol-1£¬Ņ×ČÜÓŚĖ®µÄ¹Ģ
£¬Ä¦¶ūÖŹĮæĪŖ204g•mol-1£¬Ņ×ČÜÓŚĖ®µÄ¹Ģ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 9ÖÖ | B£® | 13ÖÖ | C£® | 10ÖÖ | D£® | 11ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ņŹÖ»ś | B£® | ¹āŗĻ×÷ÓĆ | C£® | µē½āĖ® | D£® | µćČ¼ĒāĘų |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com