
工业上制CuCl2时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉(含杂质FeO)充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.
(1)在除去溶液中Fe2+时,可采用的方法是
[ ]
A.直接加碱,调整溶液pH=9.6
B.加纯铜,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3~4
D.通入H2S,使Fe2+直接沉淀
(2)工业上除去溶液中Fe2+,常使用NaClO,向溶液中加NaClO后,溶液的pH的变化是
[ ]
科目:高中化学 来源: 题型:
| aNA |
| 80 |
| b |
| 135 |
| 64b |
| 135a |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制氯化铜时,是将浓盐酸用蒸气加热至![]() CuCl2+H2O,FeO+2HCl
CuCl2+H2O,FeO+2HCl![]() FeCl2+H2O。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。?
FeCl2+H2O。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。?
(1).为除去溶液中的Fe2+,可以采用的方法是( )?
A.直接加碱,调整溶液pH≥9.6?
B.加纯铜粉,将Fe2+还原出来?
C.先将Fe2+氧化成Fe3+,再调整pH在3~4?
D.通入硫化氢,使Fe2+直接沉淀?
(2).工业上为除去溶液中的Fe2+,常使用NaClO,当向溶液中加入NaClO后,溶液pH变化情况是( )?
A.肯定减小 B.肯定增大?
C.可能减小 D.可能增大?
(3).若此溶液中只含有Fe3+时,要调整pH在3~4之间,此时最好向溶液中加入( )?
A.NaOH溶液 B.氨水?
C.CuCl2溶液 D.CuO固体?
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制氯化铜时,是将浓盐酸用蒸气加热至80 ℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌使之溶解,反应如下:CuO+2HCl====CuCl2+H2O,
FeO+2HCl====FeCl2+H2O。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3—4时,Fe3+以Fe(OH)3的形式完全沉淀。
(1)为除去溶液中的Fe2+,可以采用的方法是( )
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3—4之间
D.通入硫化氢,使Fe2+直接沉淀
(2)工业上为除去溶液中的Fe2+,常使用NaClO,当向溶液中加入NaClO后,溶液pH变化情况是( )
A.肯定减小 B.肯定增大 C.可能减小 D.可能增大
(3)若此溶液中只含有Fe3+时,要调整pH在3—4之间,此时最好向溶液中加入( )
A.NaOH溶液 B.氨水 C.CuCl2溶液 D.CuO固体
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二下学期期中考试化学试卷(带解析) 题型:填空题
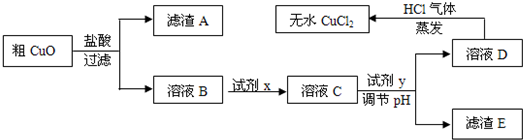
工业上制氯化铜无水物时,是将浓盐酸用蒸气加热至80 ℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁和SiO2),充分搅拌后使之溶解,制取流程如下: 已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
(1)根据常温时Fe(OH)3的Ksp计算,当溶液中的Fe3+完全沉淀(此时溶液中的Fe3+物质的量的浓度=10-5mol/L),溶液的pH= 。
(2)溶液D制取无水CuCl2时,需在HCl气体中蒸干,原因是
。
(3)粗CuO溶于过量盐酸后,得到的溶液B中加入试剂x将Fe2+氧化为Fe3+,试剂x可以是 (填以下选项序号)。
A.KMnO4溶液 B.氯水 C.NaClO溶液 D.O3
若用H2O2溶液,则反应的离子方程式为 。
(4)溶液C加入试剂y,要调整溶液的pH至3-4,试剂y不能是 (填以下选项序号),原因是 。
A.NaOH溶液 B.Cu(OH)2固体 C.Cu2(OH)2CO3固体 D.CuO固体
(5)将ag粗CuO经过以上一系列操作之后,最终得到bg无水CuCl2(不考虑实验过程中操作引起的损耗),下列说法正确的是 。(NA表示阿伏伽德罗常数)
A.粗CuO中Cu2+数目小于
B.粗CuO中CuO物质的量小于 mol
mol
C.粗CuO中所含的铜元素的质量分数为 ×100℅
×100℅
D.粗CuO中关于CuO的量无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com