
分析 第一份加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
第二份中生成的0.08mol气体为氨气,溶液中一定含有NH4+,并且物质的量为0.08mol;
第三份中4.66g沉淀为硫酸钡,12.54g沉淀为硫酸钡和碳酸钡的混合物,再根据电荷守恒,得出一定存在钾离子,据此进行解答.
解答 解:(1)第一份加入AgNO3溶液有沉淀产生,与AgNO3溶液有沉淀产生的离子有:Cl-、CO32-、SO42-,则原溶液中不一定含有Cl-,
故答案为:不一定;
(2)二份加足量NaOH溶液加热后,收集到0.08mol气体,该气体为氨气,发生反应为NH4++OH-$\frac{\underline{\;加热\;}}{\;}$NH3↑+H2O,原溶液中一定含有NH4+,并且物质的量为0.08mol,浓度为:$\frac{0.08mol}{0.1L}$=0.8mol/L,
故答案为:NH4+;0.8mol/L;
(3)不溶于盐酸的4.66g为硫酸钡,物质的量为:$\frac{4.66g}{233g/mol}$=0.02mol;12.54g沉淀是硫酸钡和碳酸钡,碳酸钡质量为12.54g-4.66g=7.88g,碳酸钡的物质的量为:$\frac{7.88g}{197g/mol}$=0.04mol,故原溶液中一定存在CO32-、SO42-,则一定没有与CO32-、SO42-反应的Mg2+、Ba2+;
再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.08mol;n(-)=2n(CO32-)+2n(SO42-)=0.12mol,正电荷总物质的量小于负电荷,故原溶液中一定有K+,至少为0.04mol,不能确定是否存在Cl-,
故答案为:BaCO3、BaSO4;CO32- 0.04mol、SO42- 0.02mol;
(4)根据以上分析可知,原溶液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K+)≥0.04mol,
故答案为:A.
点评 本题考查常见离子的检验方法,题目难度中等,注意掌握常见离子的化学性质及检验方法,本题中根据电荷守恒判断钾离子的存在为易错点,做题时需要细致分析.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:解答题
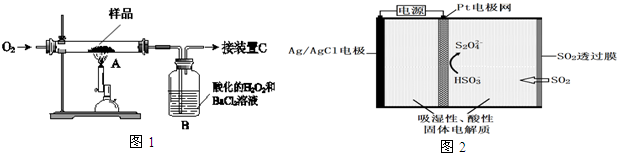
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉溶液中滴入碘水--变蓝色 | B. | 溴化银见光分解--变黑色 | ||
| C. | 苯酚溶液中滴入Fe 3+--变紫色 | D. | 胆矾空气中久置--变白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3溶液 | B. | 稀硫酸 | C. | 酚酞 | D. | Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
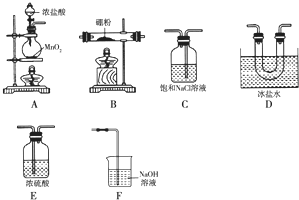
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
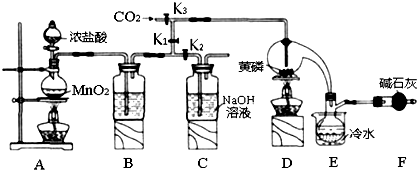
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
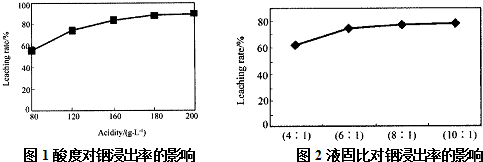

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
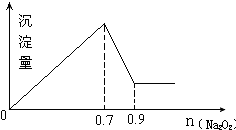
| A. | 1:3 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com