
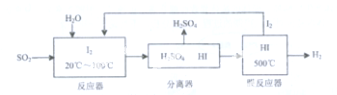
分析 Ⅰ.(1)反应器中二氧化硫、碘发生氧化还原反应生成硫酸和HI;
(2)HI分解反应为可逆反应;
Ⅱ.依据热化学方程式和盖斯定律③×2-①计算目标热化学方程式得到焓变;
Ⅲ.(1)①化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断;
②根据图象数据结合平衡常数K的计算公式进行计算;
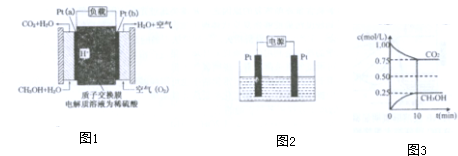
(2)①首先根据pb(a)电极上为甲醇失电子在负极发生氧化反应生成二氧化碳,据此书写电极反应式;
②整个电路中转移电子的数目相等,可以根据电子转移的数目相同来列出已知物质和未知物质之间关系式,然后通过关系来求解.
解答 解:Ⅰ.(1)反应器中二氧化硫、碘发生氧化还原反应生成硫酸和HI,离子反应为SO2+I2+2H2O=SO42-+2I-+4H+,故答案为:SO2+I2+2H2O=SO42-+2I-+4H+;
(2)HI分解反应为可逆反应,则使用膜反应器分离出H2的目的是及时分离出产物H2,有利于反应正向进行,故答案为:HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行;
Ⅱ.①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
③CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H3=-867kJ•mol-1
依据盖斯定律计算,③×2-①得到CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1;
故答案为:-1160kJ•mol-1;
Ⅲ.(1)①A.CO2的体积分数在混合气体中保持不变,则能说明达到平衡状态,故A正确;
B.平均相对分子质量=$\frac{总质量}{总物质的量}$,总质量一定,总物质的量在变,故平均相对分子质量在变,故平均相对分子质量不再发生改变能说明达到平衡状态,故B正确;
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O,不能体现正逆反应,故不能说明达到平衡状态,故C错误;
D.H2O与CH3OH都是产物,并且按照1:1的比例生成,所以H2O与CH3OH的物质的量浓度之比一直为1:1,不能说明达到平衡状态,故D错误;
故选AB;
②由图象数据CO2(g)+3H2(g)?CH3OH(g)+H2O(g)得
开始浓度:1 1.5 0 0
转化浓度:0.25 0.75 0.25 0.25
平衡浓度:0.75 0.75 0.25 0.25
所以K=$\frac{0.25×0.25}{0.75×0.75{\;}^{3}}$=0.20,故答案为:0.20;
(2)①根据pb(a)电极上为甲醇失电子在负极发生氧化反应生成二氧化碳,则电极反应式为CH3OH-6e-+H2O=CO2+6H+,故答案为:CH3OH-6e-+H2O=CO2+6H+;
②电解硫酸铜溶液时,铜电极上铜失电子发生氧化反应,当铜片的质量变化64g,失去电子的物质的量=$\frac{64g}{64g/mol}$×2=2mol,
1mol氧气生成-2价氧元素得到4mol电子,则需要空气的体积=$\frac{\frac{2mol}{4}×22.4L/mol}{20%}$=56L,
故答案为:56.
点评 本题考查氧化还原反应、电化学以及化学平衡的有关知识,为高考常见题型和高频考点,注意把握原电池的工作原理,本题解答的关键是根据电子转移的数目相同计算,注意体会答题思路,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 吸热反应一定需要加热才能发生 | |
| C. | 凡是放热反应的发生均无需加热 | |
| D. | 伴有能量变化的物质变化都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Fe | H2O(g) | Fe3O4 | H2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1.0 | 4.0 |
| C/mol | m | n | p | q |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
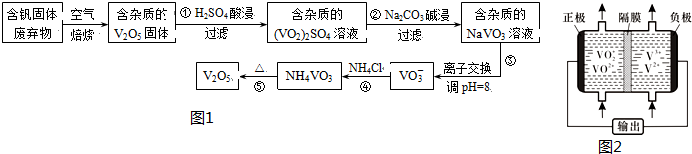
| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeO、FeS、CuO、CuS、稀硫酸 | |
| B. | 苯、四氯化碳、无水乙醇、己烯 溴水 | |
| C. | 甲酸、乙酸、乙醛、乙醇 新制氢氧化铜悬浊液 | |
| D. | 苯酚钠溶液、甲苯、乙酸乙酯、乙酸 饱和碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨是指pH<5.6雨 | |
| B. | 在正常情况下人体血液pH为7.35~7.45 | |
| C. | 有色水泥主要是因为水泥中含有CuCl2 | |
| D. | 红色玻璃主要是因为玻璃中含有少量Cu2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com