
| | 物质 | 试剂 | 分离方法 |
| ① | 硝酸钾(氯化钠) | 蒸馏水 | 降温结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 金属钠 | 蒸馏 |
| ④ | NaCl溶液(Na2S) | AgCl | 过滤 |
科目:高中化学 来源:不详 题型:单选题
| A.Fe3+ (Al3+),加过量的氨水,过滤 |
| B.KCl溶液(BaCl2),加入足量K2SO4溶液,过滤 |
| C.CO2 (SO2),饱和碳酸钠溶液,浓硫酸,洗气 |
| D.N2 [NO2(主要)、NO],NaOH溶液,浓硫酸,洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.某溶液 有白色沉淀,说明原溶液中有Cl- 有白色沉淀,说明原溶液中有Cl- |
B.某溶液 有白色沉淀,说明原溶液中有SO42- 有白色沉淀,说明原溶液中有SO42- |
C.某溶液 有蓝色沉淀,说明原溶液中有Cu2+ 有蓝色沉淀,说明原溶液中有Cu2+ |
D.某溶液 生成无色气体,说明原溶液中有CO32- 生成无色气体,说明原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
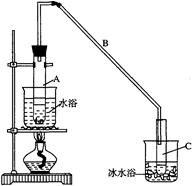

| | 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
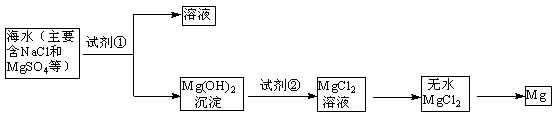
| A.N2 | B.CO2 | C.Ar | D.空气) |


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com