
| A. | 盛浓硝酸、硝酸银用棕色试剂瓶,并置于阴凉处 | |
| B. | 用带玻璃塞的磨口玻璃瓶盛氢氧化钠 | |
| C. | 金属钠通常保存在煤油里 | |
| D. | HF酸储存在塑料瓶中 |
分析 A.根据浓硝酸、硝酸银的性质确定其保存方法,浓硝酸、硝酸银易分解;
B.根据玻璃的成分及氢氧化钠、二氧化硅的性质分析;
C.根据金属钠、钾的性质来分析其保存方法;
D.氢氟酸腐蚀玻璃.
解答 解:A.浓硝酸、硝酸银是见光易分解的液体,所以通常保存在棕色细口瓶并置于阴凉处,故A正确;
B.玻璃塞的主要成分为硅酸钠、二氧化硅等,二氧化硅和氢氧化钠反应生成硅酸钠和水SiO2+2NaOH=Na2SiO3+H2O,硅酸钠是黏性物质,很容易将玻璃塞粘结,不易打开,所以盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞,故B错误;
C.钠、钾的性质很活泼,极易和空气中的氧气反应生成氧化钠和氧化钾,所以应密封保存;钠、钾的密度小于煤油的密度,且和煤油不反应,所以金属钠、钾通常保存在煤油里,故C正确;
D.氢氟酸腐蚀玻璃,所以不能放在玻璃瓶中,应储存在塑料瓶中,故D正确.
故选B.
点评 本题考查了化学试剂的存放,题目难度不大,需要掌握常见试剂的保存方法,关键是掌握试剂的性质,关键化学性质选择保存方法,试题基础性强,侧重对学生灵活运用基础知识解决实际问题的能力的培养.


科目:高中化学 来源: 题型:解答题
| 序号 | 物质 | 杂质 | 所加试剂 | 分离方法 |
| (1) | NO | NO2 | ||
| (2) | Fe粉 | Al粉 | ||
| (3) | 氯化钠固体 | 氯化铵固体 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将作物秸秆通过化学反应转化为乙醇用作汽车燃料 | |
| B. | 使用资源节约型、环境友好型的生物降解塑料包装袋 | |
| C. | 大力研发新型有机溶剂替代水作为萃取剂 | |
| D. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | MgSO4溶液中加入Ba(OH)2溶液:SO42-+Ba2+=BaSO4↓ | |
| C. | 硫化钠溶液显碱性:S2-+2H2O═H2S+2OH- | |
| D. | NaHCO3溶液加入少量Ca(OH)2溶液:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+ NH4+ SCN- Cl- | B. | Fe3+ Fe2+ Na+ NO3- | ||
| C. | Ba2+ H+ NO3- SO42- | D. | S2- Na+ ClO- OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3-、SO42-、NH4+、Mg2+ | B. | Cu2+、Mg2+、Cl-、SO42- | ||
| C. | H+、K+、OH-、NO3- | D. | Ag+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
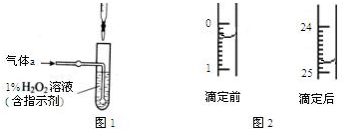
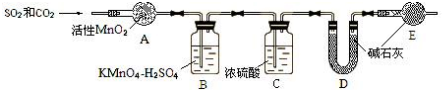
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
| A. | 当溶液pH<4,碳钢主要发生析氢腐蚀 | |
| B. | 当溶液pH>13.5,碳钢腐蚀的正极反应式为O2+4H++4e-=2H2O | |
| C. | 当溶液pH>6,碳钢主要发生吸氧腐蚀 | |
| D. | 煮沸除去氧气的碱性溶液中,碳钢腐蚀速率会减缓 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中加入1molN2和3molH2充分反应可得到NH3分子数为2NA | |
| B. | 20 g重水(D2O)中含有的电子数为10NA | |
| C. | 粗铜电解精炼时,阳极质量减少6.4 g,则转移电子数一定是0.2NA | |
| D. | 235g核素${\;}_{92}^{235}$U发生裂变反应:${\;}_{92}^{235}$U+${\;}_{0}^{1}$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$U+10${\;}_{0}^{1}$n净产生的中子(${\;}_{0}^{1}$n)数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com