
°Њћвƒњ°њ£®1£©≈®ЅтЋб”лƒЊћњЈџ‘ЏЉ”»»ћхЉюѕ¬Јі”¶µƒїѓ—ІЈљ≥ћ љќ™_______________________°£
±аЇ≈ | Ґў | ҐЏ | Ґџ | Ґ№ |
„∞÷√ |
|
|
|
|
£®2£© ‘”√±н÷–Ћщ ЊЄч„∞÷√…иЉ∆“їЄц µ—й,—й÷§…ѕ цЈі”¶Ћщ≤ъ…ъµƒЄч÷÷≤ъќп°£
’в–©„∞÷√µƒЅђљ”Ћ≥–т(∞і≤ъќп∆шЅчі”„уµљ”“µƒЈљѕт) «(ћо„∞÷√µƒ±аЇ≈)°°°°°°°°°ъ°°°°°°°°°ъ°°°°°°°°°ъ°°°°°°°°°£______________
£®3£© µ—й “÷–њ…єџ≤мµљ„∞÷√Ґў÷–A∆њµƒ»№“ЇЌ …Ђ,C∆њµƒ»№“Ї≤їЌ …Ђ°£B∆њ»№“Їµƒ„ч”√ «___________£їC∆њ»№“Їµƒ„ч”√ «________________°£
£®4£©„∞÷√ҐЏ÷–ЋщЉ”µƒєћће“©∆Ј «__________°£
£®5£©„∞÷√Ґџ÷–Ћщ Ґµƒ»№“Ї «___________£ђњ…—й÷§µƒ≤ъќп «________°£
°Њір∞Є°њ C+2H2SO4(≈®)![]() 2SO2°ь+CO2°ь+2H2O Ґ№°°ҐЏ°°Ґў°°Ґџ љЂSO2»Ђ≤њ—хїѓќь ’ —й÷§≤ъќп÷–SO2“—±їB∆њ»№“Ї»Ђ≤њ—хїѓќь ’ ќёЋЃCuSO4(їт±д…ЂєиљЇ) ≥ќ«е ѓї“ЋЃ CO2
2SO2°ь+CO2°ь+2H2O Ґ№°°ҐЏ°°Ґў°°Ґџ љЂSO2»Ђ≤њ—хїѓќь ’ —й÷§≤ъќп÷–SO2“—±їB∆њ»№“Ї»Ђ≤њ—хїѓќь ’ ќёЋЃCuSO4(їт±д…ЂєиљЇ) ≥ќ«е ѓї“ЋЃ CO2
°Њљвќц°њ£®1£©ƒЊћњ”л≈®ЅтЋб‘ЏЉ”»»ћхЉюѕ¬Јі”¶…ъ≥…ґю—хїѓћЉ°Ґґю—хїѓЅтЇЌЋЃ£ђїѓ—ІЈљ≥ћ љ£ђ2H2SO4£®≈®£©+C![]() CO2°ь+2SO2°ь+2H2O£ї
CO2°ь+2SO2°ь+2H2O£ї
£®2£©ґю—хїѓћЉЇЌґю—хїѓЅтґЉƒ№ є≥ќ«е ѓї“ЋЃ±дїл„«£ђµЂґю—хїѓЅтƒ№±їЋб–‘Єя√ћЋбЉЎ»№“Ї—хїѓґш єЋб–‘Єя√ћЋбЉЎ»№“ЇЌ …Ђ£ђƒ№ є∆ЈЇм»№“ЇЌ …ЂґшЊя”–∆ѓ∞„–‘£ђµЂґю—хїѓћЉ√ї”–іЋ–‘÷ ,Ћщ“‘Љм—йґю—хїѓћЉ÷Ѓ«∞ѕ»Љм—йґю—хїѓЅт£ђЋЃ’ф∆ш”√ќёЋЃЅтЋбЌ≠Љм—й£ђ“«∆чЅђљ”Ћ≥–т «£Ї∆шће÷∆±Є°ъЋЃ’ф∆шЉм—й°ъґю—хїѓЅтЉм—й°ъ≥э»•ґю—хїѓЅт°ъґю—хїѓЅтЉм—й°ъґю—хїѓћЉЉм—й£ђЋщ“‘∆дЅђљ”Ћ≥–т «Ґ№°ъҐЏ°ъҐў°ъҐџ£ї
£®3£©ЋЃ’ф∆шƒ№ єќёЋЃЅтЋбЌ≠”…ќё…Ђ±дќ™јґ…Ђ£ђњ…“‘”√ќёЋЃЅтЋбЌ≠Љм—йЋЃ’ф∆ш£ђЋщ“‘„∞÷√ҐЏ÷–Ћщ„∞µƒєћће“©∆Ј «ќёЋЃЅтЋбЌ≠£ђ“≤—й÷§µƒ≤ъќп «ЋЃ£ї
£®4£©ґю—хїѓћЉƒ№ є≥ќ«е ѓї“ЋЃ±дїл„«£ђЋщ“‘ µ—й “”√≥ќ«е ѓї“ЋЃЉм—йґю—хїѓћЉ£ђ‘т„∞÷√Ґџ÷–Ћщ Ґ»№“Ї «≥ќ«е ѓї“ЋЃ°£


 «бЋ…ґбєЏ»Ђƒ№’∆њЎЊнѕµЅ–ір∞Є
«бЋ…ґбєЏ»Ђƒ№’∆њЎЊнѕµЅ–ір∞Є
| ƒкЉґ | Єя÷–њќ≥ћ | ƒкЉґ | ≥х÷–њќ≥ћ |
| Єя“ї | Єя“ї√вЈ—њќ≥ћЌ∆Љц£° | ≥х“ї | ≥х“ї√вЈ—њќ≥ћЌ∆Љц£° |
| Єяґю | Єяґю√вЈ—њќ≥ћЌ∆Љц£° | ≥хґю | ≥хґю√вЈ—њќ≥ћЌ∆Љц£° |
| Єя»э | Єя»э√вЈ—њќ≥ћЌ∆Љц£° | ≥х»э | ≥х»э√вЈ—њќ≥ћЌ∆Љц£° |
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њѕ¬Ѕ– ≥ќп÷–£ђµ∞∞„÷ ЇђЅњ„оЄяµƒ «£® £©
A.Є ’бB.∆їєыC.«а≤ЋD.Љ¶µ∞
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ¬ЅЌЅњуµƒ÷ч“™≥…Ј÷ «Al2O3£ђїєЇђ”–Fe2O3°ҐSiO2µ»‘”÷ °£
Ґс£Ѓі”¬ЅЌЅњу÷–ћб»°—хїѓ¬ЅµƒЅч≥ћ»зѕ¬ЌЉЋщ Њ£Ї
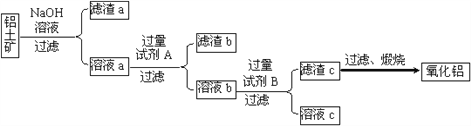
£®1£© ‘ЉЅA «________£ї»№“Їb”л ‘ЉЅBЈі”¶µƒјл„”Јљ≥ћ љќ™________°£
£®2£©Љ”»лNaOH»№“Їљш––µƒЈі”¶µƒјл„”Јљ≥ћ љќ™_________°Ґ____________°£
Ґу£Ѓ–¬–Ќћ’і…µ™їѓ¬Ѕњ…”√“‘ѕ¬Ѕљ÷÷ЈљЈ®÷∆±Є
£®3£©Ґў—хїѓ¬ЅЄяќ¬їє‘≠Ј®£Ї°°Al2O3 +°°C +°° N2 ![]() °°°°AlN +°°CO£®«л≈д∆љ£©
°°°°AlN +°°CO£®«л≈д∆љ£©
ҐЏ¬»їѓ¬Ѕ”л∞±∆шЄяќ¬Їѕ≥…Ј®£ЇAlCl3+NH3 ![]() AlN+3HCl
AlN+3HCl
£®4£©ЈљЈ®ҐЏ±»ЈљЈ®Ґў‘Џ…ъ≤ъ…ѕЄьЊя”≈ ∆°£ѕ¬Ѕ–ЋµЈ®÷–£ђ’э»Јµƒ «_______°£
A£ЃЈљЈ®Ґў÷–µƒ Al2O3°ҐC°ҐN2љбєєќ»ґ®£ђЈі”¶ ±∆∆їµїѓ—ІЉь–и“™ѕыЇƒЄьґаµƒƒ№Ѕњ
B£ЃЈљЈ®Ґў÷–µƒAl2O3ЇЌC»Ё“„≤–Ѕф‘Џµ™їѓ¬Ѕ÷–
C£ЃЅљ÷÷ЈљЈ®÷–µ™їѓ¬ЅЊщќ™їє‘≠≤ъќп
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њƒ≥…’Љо—щ∆Ј÷–Їђ”–…ўЅњ≤ї”лЋб„ч”√µƒњ…»№–‘‘”÷ £ђќ™ЅЋ≤вґ®∆діњґ»£ђљш––“‘ѕ¬µќґ®≤ў„ч£Ї
A£Ѓ‘Џ250mL»ЁЅњ∆њ÷–ґ®»Ё≥…250mL…’Љо»№“Ї
B£Ѓ”√“∆“Їє№“∆»°25mL…’Љо»№“Ї”Џ„ґ–ќ∆њ÷–≤ҐµќЉ”ЉЄµќЉ„їщ≥»÷Є ЊЉЅ
C£Ѓ‘Џћм∆љ…ѕ„Љ»Ј≥∆»°…’Љо—щ∆ЈWg£ђ‘Џ…’±≠÷–Љ”’фЅуЋЃ»№љв
D£ЃљЂќп÷ µƒЅњ≈®ґ»ќ™M mol/Lµƒ±к„ЉH2SO4»№“Ї„∞»лЋб љµќґ®є№£ђµч’ы“Ї√ж£ђЉ«ѕ¬њ™ Љњћґ»ќ™V1mL
E£Ѓ‘Џ„ґ–ќ∆њѕ¬µж“ї’≈∞„÷љ£ђµќґ®µљ÷’µг£ђЉ«¬Љ÷’µгњћґ»ќ™V2mL
їЎірѕ¬Ѕ–ќ ћв£Ї
£®1£©’э»Јµƒ≤ў„ч≤љ÷иµƒЋ≥–т «£®”√„÷ƒЄћо–і£© £Ѓ
£®2£©µќґ®є№ґЅ э”¶„Ґ“в £Ѓ
£®3£©≤ў„чE÷–µƒ„ґ–ќ∆њѕ¬µж“ї’≈∞„÷љµƒ„ч”√ « £Ѓ
£®4£©≤ў„чD÷–“Ї√收µч’ыµљ £ђ Љв„м≤њЈ÷”¶ £Ѓ
£®5£©µќґ®÷’µг ±„ґ–ќ∆њƒЏ»№“ЇµƒpH ‘Љќ™ £ђ ÷’µг ±—’…Ђ±дїѓ « £Ѓ
£®6£©»фЋб љµќґ®є№√ї”–”√±к„ЉH2SO4»уѕі£ђїбґ‘≤вґ®љбєы”–Їќ”∞ѕм£®ћо°∞∆ЂЄя°±°∞∆ЂµЌ°±їт°∞ќё”∞ѕм°±£ђ∆дЋь≤ў„чЊщ’э»Ј£©
£®7£©Є√…’Љо—щ∆Јµƒіњґ»Љ∆Ћг љ « £Ѓ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њƒ≥…’Љо—щ∆Ј÷–Їђ”–…ўЅњ≤ї”лЋб„ч”√µƒњ…»№–‘‘”÷ £ђќ™ЅЋ≤вґ®∆діњґ»£ђљш––“‘ѕ¬µќґ®≤ў„ч£Ї
A£Ѓ‘Џ250mL»ЁЅњ∆њ÷–ґ®»Ё≥…250mL…’Љо»№“Ї
B£Ѓ”√“∆“Їє№“∆»°25mL…’Љо»№“Ї”Џ„ґ–ќ∆њ÷–≤ҐµќЉ”ЉЄµќЉ„їщ≥»÷Є ЊЉЅ
C£Ѓ‘Џћм∆љ…ѕ„Љ»Ј≥∆»°…’Љо—щ∆ЈWg£ђ‘Џ…’±≠÷–Љ”’фЅуЋЃ»№љв
D£ЃљЂќп÷ µƒЅњ≈®ґ»ќ™M mol/Lµƒ±к„ЉH2SO4»№“Ї„∞»лЋб љµќґ®є№£ђµч’ы“Ї√ж£ђЉ«ѕ¬њ™ Љњћґ»ќ™V1mL
E£Ѓ‘Џ„ґ–ќ∆њѕ¬µж“ї’≈∞„÷љ£ђµќґ®µљ÷’µг£ђЉ«¬Љ÷’µгњћґ»ќ™V2mL
їЎірѕ¬Ѕ–ќ ћв£Ї
£®1£©’э»Јµƒ≤ў„ч≤љ÷иµƒЋ≥–т «£®”√„÷ƒЄћо–і£© £Ѓ
£®2£©µќґ®є№ґЅ э”¶„Ґ“в £Ѓ
£®3£©≤ў„чE÷–µƒ„ґ–ќ∆њѕ¬µж“ї’≈∞„÷љµƒ„ч”√ « £Ѓ
£®4£©≤ў„чD÷–“Ї√收µч’ыµљ £ђ Љв„м≤њЈ÷”¶ £Ѓ
£®5£©µќґ®÷’µг ±„ґ–ќ∆њƒЏ»№“ЇµƒpH ‘Љќ™ £ђ ÷’µг ±—’…Ђ±дїѓ « £Ѓ
£®6£©»фЋб љµќґ®є№√ї”–”√±к„ЉH2SO4»уѕі£ђїбґ‘≤вґ®љбєы”–Їќ”∞ѕм£®ћо°∞∆ЂЄя°±°∞∆ЂµЌ°±їт°∞ќё”∞ѕм°±£ђ∆дЋь≤ў„чЊщ’э»Ј£©
£®7£©Є√…’Љо—щ∆Јµƒіњґ»Љ∆Ћг љ « £Ѓ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њA°ҐB°ҐC°ҐD°ҐEќе÷÷ќпЈ÷±р «NaOH°ҐNH3H2O°ҐCH3COOH°ҐHCl°ҐNH4HSO4÷–µƒ“ї÷÷£Ѓ≥£ќ¬ѕ¬љш––ѕ¬Ѕ– µ—й£Ї
Ґў0.001mol/LµƒA»№“ЇpH=3£ї
ҐЏB»№“ЇЇЌD»№“Їѕ‘Љо–‘£ђµ»≈®ґ»Ѕљ’яPHєЎѕµB£ЉD£ї
ҐџE «»хµзљв÷ £ЃїЎірѕ¬Ѕ–ќ ћв£Ї
£®1£©D «»№“Ї£ђ≈–ґѕјн”… « £Ѓ
£®2£©”√ЋЃѕ° Ќ0.1molL©Б1 B ±£ђ»№“Ї÷–Ћж„≈ЋЃЅњµƒ‘цЉ”ґшЉх–°µƒ «£®ћо–і–тЇ≈£©£Ѓ
Ґў ![]() ҐЏ
ҐЏ ![]() Ґџc£®H+£©ЇЌc£®OH©Б£©µƒ≥Ћїэ Ґ№OH©Бµƒќп÷ µƒЅњ
Ґџc£®H+£©ЇЌc£®OH©Б£©µƒ≥Ћїэ Ґ№OH©Бµƒќп÷ µƒЅњ
£®3£©љЂµ»ћеїэ°Ґµ»ќп÷ µƒЅњ≈®ґ»BЇЌCµƒ»№“ЇїмЇѕ£ђ…эЄяќ¬ґ»£®»№÷ ≤їїбЈ÷љв£©»№“ЇpHЋжќ¬ґ»±дїѓќ™ЌЉ÷–µƒ«ъѕя£®ћо–і–тЇ≈£©£Ѓ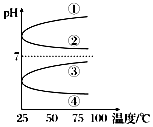
£®4£©OH©Б≈®ґ»ѕаЌђµƒµ»ћеїэµƒЅљЈЁ»№“ЇAЇЌE£ђЈ÷±р”л–њЈџЈі”¶£ђ»ф„оЇуљц”–“їЈЁ»№“Ї÷–іж‘Џ–њ£ђЈ≈≥ц«в∆шµƒ÷ ЅњѕаЌђ£ђ‘тѕ¬Ѕ–ЋµЈ®’э»Јµƒ «£®ћо–і–тЇ≈£©£Ѓ
ҐўЈі”¶Ћщ–и“™µƒ ±ЉдE£ЊA
ҐЏњ™ ЉЈі”¶ ±µƒЋў¬ A£ЊE
Ґџ≤ќЉ”Јі”¶µƒ–њµƒќп÷ µƒЅњA=E
Ґ№Јі”¶єэ≥ћµƒ∆љЊщЋў¬ E£ЊA
ҐЁA»№“Їјп”––њ £”а
ҐёE»№“Їјп”––њ £”а£Ѓ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њµЏIIA„е‘™ЋЎЊя”–ѕаЋ∆µƒїѓ—І–‘÷ £ђ «”…”ЏЋь√«µƒ‘≠„”Њя”–ѕаЌђµƒ
A£Ѓ‘≠„”∞лЊґ B£Ѓµз„”≤г э C£ЃЇЋЌвµз„” э D£Ѓ„оЌв≤гµз„” э
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њєЎ”ЏЈі”¶2KI+O3+H2O ==2KOH+I2+O2£ђѕ¬Ѕ–ЋµЈ®’э»Јµƒ «
A£Ѓµ±”–2 molKI±ї—хїѓ ±£ђ2 mol—х‘≠„”±їїє‘≠
B£ЃO2 «їє‘≠≤ъќп
C£Ѓ»фѕыЇƒ2.24 L O3£ђ‘т„™“∆0.2 molµз„”
D£Ѓ—хїѓЉЅ”лїє‘≠≤ъќпµƒќп÷ µƒЅњ÷Ѓ±»ќ™1:1
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ±нќ™‘™ЋЎ÷№∆Џ±н÷–µƒ“ї≤њЈ÷£ђЅ–≥цЅЋ10÷÷‘™ЋЎ‘Џ‘™ЋЎ÷№∆Џ±н÷–µƒќї÷√£Ѓ”√їѓ—ІЈыЇ≈їЎірѕ¬Ѕ–Єчќ ћв£Ѓ
÷ч„е | ||||||||
÷№∆Џ | Ґс | Ґт | Ґу | Ґф | Ґх | Ґц | Ґч | 0 |
2 | Ґё | Ґя | ||||||
3 | Ґў | Ґџ | ҐЁ | Ґа | Ґв | |||
4 | ҐЏ | Ґ№ | Ґб |
£®1£©10÷÷‘™ЋЎ÷–£ђµЏ“їµзјлƒ№„оіуµƒ «£їµзЄЇ–‘„о–°µƒљр ф « £Ѓ
£®2£©Ґў°ҐҐџ°ҐҐЁ»э÷÷‘™ЋЎ„оЄяЉџ—хїѓќпґ‘”¶µƒЋЃїѓќп÷–£ђЉо–‘„о«њµƒ « £Ѓ
£®3£©ҐЏ°ҐҐџ°ҐҐ№»э÷÷‘™ЋЎ–ќ≥…µƒјл„”£ђјл„”∞лЊґ”…іуµљ–°µƒЋ≥–т «£Ї £Ѓ
£®4£©ҐўЇЌҐбµƒ„оЄяЉџ—хїѓќпґ‘”¶ЋЃїѓќпµƒїѓ—І љќ™ЇЌ £Ѓ ҐўЇЌҐбЅљ‘™ЋЎ–ќ≥…їѓЇѕќпµƒїѓ—І љќ™£їЄ√їѓЇѕќп„∆…’ ±µƒ—ж…Ђќ™…Ђ£їЄ√їѓЇѕќпµƒ»№“Ї”л‘™ЋЎҐаµƒµ•÷ Јі”¶µƒїѓ—ІЈљ≥ћ љќ™ £Ѓ
£®5£©ҐўЇЌҐЁ„оЄяЉџ—хїѓќпґ‘”¶ЋЃїѓќпѕаї•Јі”¶µƒїѓ—ІЈљ≥ћ љќ™£їјл„”Јљ≥ћ љќ™ £Ѓ
£®6£©”√µз„” љ±н ЊµЏ»э÷№∆Џ‘™ЋЎ÷–”…µзЄЇ–‘„о–°µƒ‘™ЋЎЇЌµзЄЇ–‘„оіуµƒ‘™ЋЎ–ќ≥…їѓЇѕќпµƒєэ≥ћ £Ѓ
≤йњіір∞ЄЇЌљвќц>>
∞ўґ»÷¬–≈ - ЅЈѕ∞≤бЅ–±н - ‘ћвЅ–±н
Їю±± °ї•Ѕ™Ќшќ•Ј®ЇЌ≤їЅЉ–≈ѕҐЊў±®∆љћ® | Ќш…ѕ”–Ї¶–≈ѕҐЊў±®„®«ш | µз–≈’©∆≠Њў±®„®«ш | …жјъ Ј–йќё÷ч“е”–Ї¶–≈ѕҐЊў±®„®«ш | …ж∆у«÷»®Њў±®„®«ш
ќ•Ј®ЇЌ≤їЅЉ–≈ѕҐЊў±®µзї∞£Ї027-86699610 Њў±®” ѕд£Ї58377363@163.com