
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 有机物M的分子式为C4H8O3,相同条件下,等量的M分别与足量的碳酸氢钠溶液、钠完全反应,产生等体积的CO2和H2.说明有机物分子中含有1个羧基,1个羟基,先写出丁酸的同分异构体,然后连接上羟基,以此判断同分异构体.
解答 解:说明有机物分子中含有1个羧基,1个羟基,丁酸的同分异构体:CH3CH2CH2COOH,CH3CH(CH3)COOH,连接上羟基可得同分异构体:CH2OHCH2CH2COOH,CH3CHOHCH2COOH,CH3CH2CHOHCOOH,CH2OHCH(CH3)COOH,CH3COH(CH3)COOH,共有5种,
故选C.
点评 本题考查有机物推断及同分异构体种类判断,为高频考点,侧重考查学生的分析能力,明确常见有机物官能团性质是解本题关键,难点是同分异构体种类判断,要考虑碳链异构、位置异构,题目难度不大.


科目:高中化学 来源:2017届甘肃省高三上学期期中化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B.Na2CO3溶液中CO32-的水【解析】
CO32-+H2O=HCO3-+OH-
C.酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D.NaHCO3溶液中加过量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
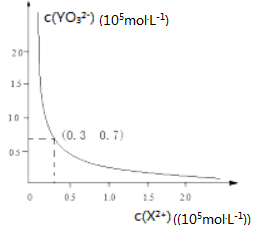
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 | |
| B. | 在一定条件下,苯与液溴、浓硝酸、浓硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 | |
| C. | 将少量钠投入到盛有水和乙醇的烧杯中,比较水和乙醇中氢的活泼性 | |
| D. | 聚合物 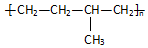 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
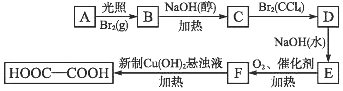
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com