
| A. | NaCl的电子式: | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | CO2的分子模型示意图: | D. | O2-的离子结构示意图: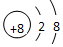 |
分析 A.氯化钠为离子化合物,钠离子与氯离子通过离子键结合;
B.次氯酸分子中氧原子分别于氢原子、氯原子各共用1对电子;
C.二氧化碳为直线形分子;
D.氧离子核内有8个质子,核外10个电子,两个电子层,分别容纳电子数2,8;
解答 解:A.氯化钠为离子化合物,钠离子与氯离子通过离子键结合,电子式: ,故A错误;
,故A错误;
B.次氯酸分子中氧原子分别于氢原子、氯原子各共用1对电子,结构式为:H-O-Cl,故B错误;
C.二氧化碳为直线形分子,三个原子在一条直线上,故C错误;
D.氧离子核内有8个质子,核外10个电子,两个电子层,分别容纳电子数2,8,O2-的离子结构示意图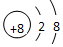 ,故D正确;
,故D正确;
故选:D.
点评 本题是一道综合知识的考查题目,涉及原子结构、电子式、原子结构示意图,要求学生具有分析和解决问题的能力,注意平时知识的积累是解题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 过氧化氢电子式: | B. | F-的结构示意图: | ||
| C. | 邻羟基苯甲酸的结构简式: | D. | 中子数为28的钙原子:${\;}_{20}^{28}$Ca |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 墨水是一种胶体,不同墨水混用时可能使钢笔流水不畅或者堵塞 | |
| B. | 持续加热到一定温度能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 洁厕液与84消毒液混合洗厕所可以达到洗涤和消毒杀菌的双重功效,对人体不可能造成伤害 | |
| D. | 用13C示踪原子法可以进行幽门螺旋杆菌的精确检测 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
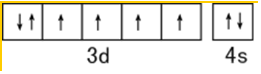 .
.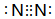 .
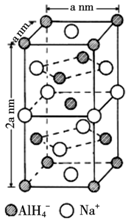
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
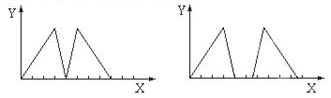
| A. | 三溴化铝溶液 | B. | 偏铝酸钠溶液 | C. | 明矾溶液 | D. | 硝酸铝溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.
将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急.| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.8 g | B. | 19.2 g | C. | 32.0 g | D. | 38.4 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com