
【题目】电解NO制备NH4NO3的工作原理如图所示,X、Y均为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A。下列说法正确的是( )

A.物质A为HNO3
B.X电极为阳极
C.利用该装置电解2molNO理论上可生成1.25molNH4NO3
D.Y电极反应式为NO-3e-+4OH-=NO3-+2H2O
【答案】C
【解析】
电解NO制备NH4NO3,Y为阳极反应为NO-3e-+2H2O=NO3-+4H+,X为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为: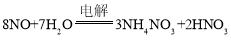 ,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此分析.
,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此分析.
A.根据以上分析,则A为NH3,故A错误;
B.根据以上分析,X电极为电解池阴极,故B错误;
C.补充NH3后总反应方程式变为: ,根据方程式可知电解8molNO理论上产生5mol NH4NO3,所以利用该装置电解2molNO理论上可生成1.25molNH4NO3,故C正确;
,根据方程式可知电解8molNO理论上产生5mol NH4NO3,所以利用该装置电解2molNO理论上可生成1.25molNH4NO3,故C正确;
D.Y为阳极反应为:NO-3e-+2H2O=NO3-+4H+,故D错误;
故选:C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的化学方程式为___,工艺师常用___(填物质名称或化学式)来雕刻玻璃。
(2)用Na2SiO3溶液浸泡过的棉花不易燃烧,体现Na2SiO3的用途可作___的原料。
(3)工业上常用2C+SiO2![]() Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是___(填化学式,下同),氧化剂是___。
Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是___(填化学式,下同),氧化剂是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。

回答下列问题:
(1)图B对应的物质名称是_________,其晶胞中的原子数为______,晶体类型为_______。
(2)d中元素的原子核外电子排布式为_______。
(3)图A中由二种元素组成的物质中,沸点最高的是______,原因是______,该物质的分子构型为_________,中心原子的杂化轨道类型为_________。
(4)图A中的双原子分子中,极性最大的分子是_________。
(5)k的分子式为_________,中心原子的杂化轨道类型为_________,属于_________分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸钴[ Cox(OH)y(CO3)z ]常用作电子材料,磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
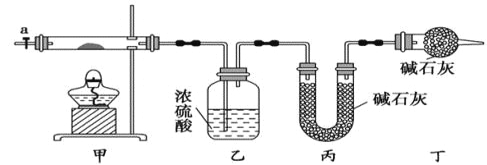
(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中____________(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是_____________________
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的______(填字母)连接在_________(填装置连接位置)。
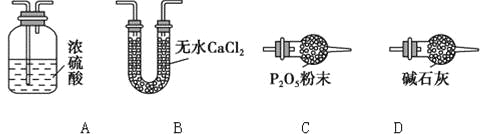
(4)若按正确装置进行实验,测得如下数据:
乙装置的质量/g | 丙装置的质量/g | |
加热前 | 80.00 | 62.00 |
加热后 | 80.36 | 62.88 |
则该碱式碳酸钴的化学式为_________________。
(5)含有Co(AlO2)2的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为___________。
(6)CoCl2·6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种工艺如下:
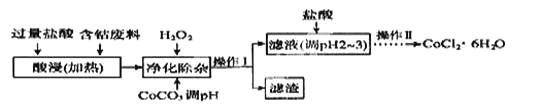
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | CO(OH)2 | Al(OH)2 |
开始沉淀(PH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(PH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净除杂质时,加入H2O2 发生反应的离子方程式为______________。
②加入CoCO3调PH为5.2~7.6,则操作Ⅰ获得的滤渣成分为
③加盐酸调整PH为2~3的目的为__________________________________。
④操作Ⅱ过程为___________(填操作名称)、过滤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.SiO2![]() H2SiO3
H2SiO3![]() Na2SiO3
Na2SiO3
B.饱和食盐水![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)
C.海水![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgCl2(aq)
MgCl2(aq)![]() Mg(s)
Mg(s)
D.NH3![]() N2
N2![]() HNO3
HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吗替麦考酚酯主要用于预防同种异体的器官排斥反应,其结构简式如下图所示。

下列说法正确的是
A. 吗替麦考酚酯的分子式为C23H30O7N
B. 吗替麦考酚酯可发生加成、取代、消去反应
C. 吗替麦考酚酯分子中所有碳原子一定处于同一平面
D. 1mol吗替麦考酚酯与NaOH溶液充分反应最多消耗3mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相对分子质量为70的烯烃的分子式为___;若该烯烃与足量的H2加成后生成分子为含3个甲基的烷烃A,则该烯烃可能的结构简式为___(任写其中一种)。若A的一种同分异构体B常温常压下为气体,一氯代物只有一种结构,B的二氯代物有___种。0.5molB的二氯代物最多可与___molCl2在光照条件下发生取代反应。
(2)有机物C的结构简式为![]() ,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个非常对称的分子构型,写出C的该种同分异构体的结构简式___,用系统命名法命名为___。
,若C的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个非常对称的分子构型,写出C的该种同分异构体的结构简式___,用系统命名法命名为___。
(3)烯烃D是2-丁烯的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁烷,D分子中能够共平面的碳原子个数最多为___个,D使溴的四氯化碳溶液褪色的反应类型是___,产物的结构简式为___;一定条件下D能发生加聚反应,写出其化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有Fe2O3、CuO、SiO2等杂成) 制备ZnSO4 ·7H2O的流程如下。
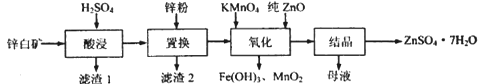
相关金属离了生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 6.4 | 8.0 |
(1)“滤渣1”的主要成分为_________(填化学式)。“酸浸”过程中,提高锌元素浸出率的措施有:适当提高酸的浓度、______________(填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+,H+反应外,另一主要反应的化学方程式为__________________________。
(3)“氧化”一步中,发生反应的离子方程式为_______________________。溶液pH控制在[3.2,6.4)之间的目的是________________。
(4)“母液”中含有的盐类物质有_________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、Al、O、N、S、Fe是常见的六种元素。
(1)S位于元素周期表______周期第______族,Fe的基态原子核外价电子排布式为______;O的基态原子核外有______种运动状态不同的电子。
(2)用“>”“<”或“=”填空
第一电离能 | 氧化性 | 沸点 | 非金属性 |
N______S | Fe3+______ Al3+ | NH3______H2O | 16O______18O |
(3)已知:下列两个热化学方程式:
4Fe(s)+302(g)=2Fe2O3(s)△H=﹣a kJ/mol
4Al(s)+3O2(g)=2Al2O3(s)△H=﹣b kJ/mol
则Al(s)的单质和Fe2O3(s)反应的热化学方程式是______。
(4)FeSO4溶液可与硝酸发生反应,写出此反应的离子方程式,并标出电子转移的方向和数目____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com