
| X | Y | Z | |
| A | FeCl2溶液 | FeCl3 | KSCN溶液 |
| B | Fe粉 | A1粉 | NaOH溶液 |
| C | Fe2(SO4)3溶液 | FeS04 | C12 |
| D | FeCl2溶液 | CuCl2 | Zn粉 |
| A、A、 | B、B、 | C、C、 | D、D、 |


科目:高中化学 来源: 题型:
| A、64g SO2含有氧原子数为1NA |
| B、物质的量浓度为0.5mol/L Mg Cl2溶液,含有Cl-离子数为1NA |
| C、0.5NA个O2的质量为32g |
| D、常温常压下,14g N2含有分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
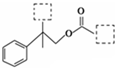 所示(其中虚线框内为未知部分的结构),A可发生如下转化(其中部分产物已略去).
所示(其中虚线框内为未知部分的结构),A可发生如下转化(其中部分产物已略去).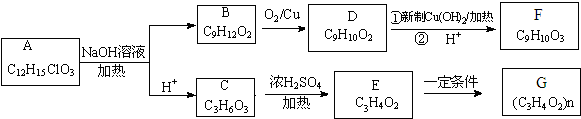
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:| 36.5a |
| 22.4(a+b)d |
| 1000aI |
| 36.5a+22.4 |
| ad |
| 36.5a+22400 |
| 1000ad |
| 36.5a+22400 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑦ | B、②⑤⑥ |
| C、①④⑦ | D、③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
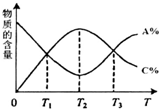 向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)?cC(g).反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是( )
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)?cC(g).反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1、T3温度时达到过化学平衡 |
| B、该反应在T2温度时达到过化学平衡 |
| C、该反应的逆反应是放热反应 |
| D、升高温度,平衡会向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com