
【题目】环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中 F 可以作内燃机的抗冻剂,J 分子中无饱和碳原子。已知:R1—CH==CH—R2→R1—CHO+R2—CHO
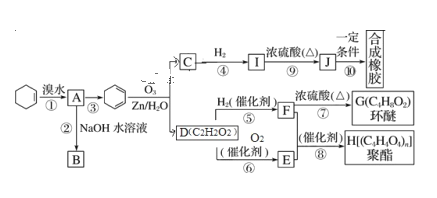
(1)A的结构简式为_____③的反应试剂及条件是______
(2)有机物B和 I的关系为_____(填字母)。
A.同系物 B.同分异构体 C.都属于醇类 D.都属于烃
(3)H的名称_________
(4)写出下列反应的化学方程式并注明反应类型:
反应⑨_________;________
(5)写出两种C的属于酯类的链状同分异构体的结构简式:_________;________
(6)参照题给信息,试写出以 2-丁烯为原料制取乙酸乙酯的合成路线流程图(无机原料任选)
_____________________
【答案】![]() NaOH的醇溶液 C 聚乙二酸乙二酯 HOCH2CH2CH2OH
NaOH的醇溶液 C 聚乙二酸乙二酯 HOCH2CH2CH2OH![]() CH2=CHCH=CH2+2H2O 消去反应 CH2=CHCOOCH3 HCOOCH2CH=CH2
CH2=CHCH=CH2+2H2O 消去反应 CH2=CHCOOCH3 HCOOCH2CH=CH2 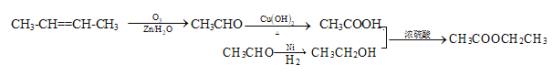
【解析】
环己烯![]() 与溴发生加成反应生成A
与溴发生加成反应生成A![]() ,A在氢氧化钠水溶液,加热条件下发生水解反应生成B为
,A在氢氧化钠水溶液,加热条件下发生水解反应生成B为![]() ,A发生消去反应生成
,A发生消去反应生成![]() ,
,![]() 发生信息中反应生成OHCH2CH2CHO、OHCCHO,C与氢气发生加成反应生成F为醇,D发生氧化反应生成E为羧酸,故F、E含有一相同的碳原子数目,由F发生取代反应生成环醚G的分子式可知,D中含有2个碳原子,则C为OHCH2CH2CHO,D为OHCCHO,则F为HOCH2CH2OH,E为HOOCCOOH,2分子HOCH2CH2OH发生脱水反应生成环醚G为
发生信息中反应生成OHCH2CH2CHO、OHCCHO,C与氢气发生加成反应生成F为醇,D发生氧化反应生成E为羧酸,故F、E含有一相同的碳原子数目,由F发生取代反应生成环醚G的分子式可知,D中含有2个碳原子,则C为OHCH2CH2CHO,D为OHCCHO,则F为HOCH2CH2OH,E为HOOCCOOH,2分子HOCH2CH2OH发生脱水反应生成环醚G为![]() ,F、E通过酯化反应进行的缩聚反应生成聚酯H为
,F、E通过酯化反应进行的缩聚反应生成聚酯H为![]() ,C与氢气发生加成反应生成I为HOCH2CH2CH2OH,I在浓硫酸、加热条件下生成J,J分子中无饱和碳原子,应发生消去反应,可推知J 为CH2=CHCH=CH2,J发生加聚反应得到合成橡胶
,C与氢气发生加成反应生成I为HOCH2CH2CH2OH,I在浓硫酸、加热条件下生成J,J分子中无饱和碳原子,应发生消去反应,可推知J 为CH2=CHCH=CH2,J发生加聚反应得到合成橡胶![]() ,据此解答。
,据此解答。
(1)由分析可知A的结构式为:![]() ;A发生消去反应生成
;A发生消去反应生成![]() ,消去反应的条件和试剂是:NaOH的醇溶液;
,消去反应的条件和试剂是:NaOH的醇溶液;
(2)B为![]() ,I为HOCH2CH2CH2OH,都是醇类;故选C;
,I为HOCH2CH2CH2OH,都是醇类;故选C;
(3)由分析可知H为![]() ,基本单位是:HOOCCOOCH2CH2OH,名称是乙二酸乙二酯,故聚合体名称是:聚乙二酸乙二酯;
,基本单位是:HOOCCOOCH2CH2OH,名称是乙二酸乙二酯,故聚合体名称是:聚乙二酸乙二酯;
(4)I为HOCH2CH2CH2OH,I在浓硫酸、加热条件下生成J,J分子中无饱和碳原子,应发生消去反应,可推知J 为CH2=CHCH=CH2,方程式为:HOCH2CH2CH2OH![]() CH2=CHCH=CH2+2H2O;该反应是消去反应;
CH2=CHCH=CH2+2H2O;该反应是消去反应;
(5)C的分子式为:C2H2O2,其酯类的链状同分异构体的结构简式有:CH2=CHCOOCH3,HCOOCH2CH=CH2,HCOOCH=CHCH3;
(6)结合题目所给信息:R1—CH==CH—R2→R1—CHO+R2—CHO可以设计如下合成路线: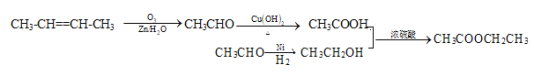 。
。


科目:高中化学 来源: 题型:
【题目】![]() 铜镁合金完全溶解于50mL密度为
铜镁合金完全溶解于50mL密度为![]() 、质量分数为
、质量分数为![]() 的浓硝酸中,得到
的浓硝酸中,得到![]() 和
和![]() 的混合气体
的混合气体![]() ,向反应后的溶液中加入
,向反应后的溶液中加入![]() NaOH溶液,当金属离子全部沉淀时,得到
NaOH溶液,当金属离子全部沉淀时,得到![]() 沉淀。下列说法不正确的是
沉淀。下列说法不正确的是![]()
A.该合金中铜与镁的物质的量之比是2:1
B.得到![]() g沉淀时,加入NaOH溶液的体积是600mL
g沉淀时,加入NaOH溶液的体积是600mL
C.![]() 和
和![]() 的混合气体中,
的混合气体中,![]() 的体积分数是
的体积分数是![]()
D.该浓硝酸中![]() 的物质的量浓度是
的物质的量浓度是![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。回答下列问题:
(1)Ag与Cu在同一族,则Ag在周期表中_____(填“s”、“p”、“d”或“ds”)区。[Ag(NH3)2]+中Ag+空的5s轨道和5p轨道以sp杂化成键,则该配离子的空间构型是_____。
(2)表中是Fe和Cu的部分电离能数据:请解释I2(Cu)大于I2(Fe)的主要原因:______。
元素 | Fe | Cu |
第一电离能I1/kJ·mol-1 | 759 | 746 |
第二电离能I2/kJ·mol-1 | 1561 | 1958 |
(3)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是______;1mol该配离子中含σ键数目为______。
②该配合物中存在的作用力类型有______(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(4)MnO的熔点(1660℃)比MnS的熔点(1610℃)高,其主要原因是________。
(5)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(CH3NH3PbI3)半导体作为吸光材料,CH3NH3PbI3具有钙钛矿(AMX3)的立方结构,其晶胞如图所示。
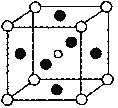
①AMX3晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M处于_______位置,X处于______位置(限选“体心”、“顶点”、“面心”或“棱心”进行填空)。
③CH3NH3PbI3晶体的晶胞参数为a nm,其晶体密度为dg·cm-3,则阿伏加德罗常数的值NA的计算表达式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:

已知以下信息:① A的核磁共振氢谱表明其只有一种化学环境的氢;
②R—CH=CH2![]() R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的化学名称为______________。
(2)D的结构简式为_____________。
(3)E的分子式为_________________。
(4)F生成G的化学方程式为________________________,该反应类型为__________。
(5)I的结构筒式为____________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,符合以上条件的同分异构体共有___________种。
J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释过程或事实的方程式不正确的是( )
A.氯气用于自来水消毒:Cl2+H2O=HCl+HClO
B.铁可以和稀硫酸反应:2Fe+3H2SO4=Fe2(SO4)3 +3H2↑
C.刻制印刷电路板时常用氯化铁溶液作为“腐蚀液”刻蚀铜板 2Fe3++Cu=2Fe2++ Cu2+.
D.红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe + 4H2O(g)![]() Fe3O4 + 4H2
Fe3O4 + 4H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)( )
A.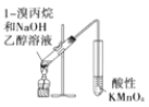 用于检验溴丙烷消去产物
用于检验溴丙烷消去产物
B.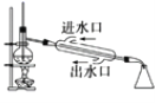 用于石油的分馏
用于石油的分馏
C.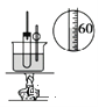 用于实验室制硝基苯
用于实验室制硝基苯
D.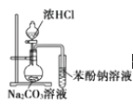 可证明酸性:盐酸>碳酸>苯酚
可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2·12H2O(铵明矾)可用作泡沫灭火器的内留剂、石油脱色剂等。某兴趣小组同学用氧化铁、铝粉、镁条和氯酸钾等物质做铝热反应的铝灰及硫酸铵等为原料制备铵明矾的实验,步骤如下:

(1)下列有关说法中正确的是__(填字母)。
A.“滤液1”中含有K+、Mg2+、Cl-
B.“滤渣1”和“滤渣2”中含有相同的物质
C.“滤渣2”中含有氢氧化铁,氢氧化镁等固体
D.将“滤液3”蒸干并灼烧,可得纯碱
(2)用NaOH溶解“滤渣1”时,可以采用__方式提高浸出率。
(3)用NaOH溶解“滤渣1”时,可能发生的反应的化学方程式为①__、②_____。
(4)向“滤液2”中通入足量的CO2,写出相应的离子反应方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。测得H2的物质的量随时间变化如图所示(图中字母后的数字表示对应的坐标)。该反应在8~10 min内CO2的平均反应速率是
CH3OH(g)+H2O(g) ΔH<0。测得H2的物质的量随时间变化如图所示(图中字母后的数字表示对应的坐标)。该反应在8~10 min内CO2的平均反应速率是

A. 0.5 mol·L-1·min-1B. 0.1 mol·L-1·min-1
C. 0 mol·L-1·min-1D. 0.125 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z在周期表中位置关系如图所示
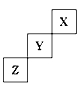
(1)X元素的名称是___________。
(2)Y在元素周期表中的位置是__________,它形成单质的化学式是_________。
(3)Z元素的原子结构示意图为__________。写出Z单质与铁反应的化学反应方程式:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com