
向1LFeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br一)=3c(Cl一),反应过程中溶液的体积变化忽略不计,则下列说法中正确的是( )
A.原溶液的浓度为0.1mol/L B.反应后溶液中c(Fe3+)=0.1mol/L
C.反应后溶液中c(Fe3+)=c(Fe2+) D.原溶液中c(Br一)=0.4mol/L
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2015-2016学年浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
分别用X、Y、Z、W四种金属进行如下三个实验:
1 | 将X与Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
2 | 将X、W分别投入等浓度的稀盐酸中都有气体产生,但W比X反应剧烈 |
3 | 用惰性电极电解含等物质的量浓度的Y2+和Z2+混合溶液,在阴极上首先析出单质Z |
根据以上事实的下列判断错误的是
A.Z的阳离子氧化性最强
B.W的还原性强于Y的还原性
C.Z放入CuSO4溶液中一定有Cu析出
D.用X、Z和稀硫酸构成的原电池,X做负极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:选择题
在下列条件下,两种气体的分子数一定相等的是 ( )
A.同密度、同压强的N2和C2H4 B.同温度、同体积的O2和N2
C.同体积、同密度的C2H4和CO D.同压强、同体积的O2和N2
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第四次月考理综化学试卷(解析版) 题型:填空题
【化学一选修3:物质结构与性质】
随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
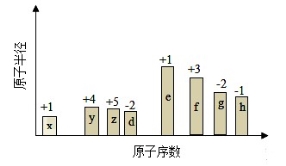
根据判断出的元素回答问题:
(1)f在元素周期表的位置是____。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_ _>____;比较g、h的最高价氧化物对应的水化物的酸性强弱是:__ _>_ _。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________________。
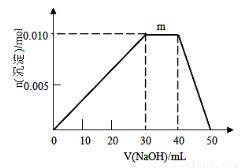
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:①R离子浓度由大到小的顺序是:______ _。②写出m点反应的离子方程_ 。③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:选择题
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
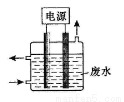
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C.阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + 5Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测一化学试卷(解析版) 题型:选择题
己知在碱性溶液中可发生如下反应:
2R(OH)3 + 3C1O- + 4OH- = 2RO4n-+3Cl- +5H2O则RO4n-中R的化合价是( )
A.+3 B +4 C.+5 D.+6
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上12月月考化学试卷(解析版) 题型:选择题
在一定温度下可逆反应N2+3H2 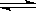 2NH3已达到平衡,下列有关说法正确的 ( )
2NH3已达到平衡,下列有关说法正确的 ( )
①1个N≡N键断裂的同时,有3个H—H键形成
②反应混合物中各组分的体积分数保持不变
③恒温恒容时,容器内的压强不再改变
④1个N≡N键断裂的同时,有3个N—H键形成
⑤NH3生成的速率与NH3分解的速率相等
⑥单位时间生成nmolN2,同时生成2nmolNH3
⑦气体的平均相对分子质量不再改变
⑧N2H2NH3的分子数一定为1∶3∶2
⑨恒温恒容时,气体的总物质的量不再改变
⑩恒温恒压时,容器内的密度不再改变
A、①②③④⑤⑥⑦⑨ B、①②③⑤⑥⑩ C、③④⑤⑥⑦ ⑧ D、①②③⑤⑥⑦⑨⑩
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期末考试化学试卷(解析版) 题型:计算题
计算题:将0.2molMg、Al的混合物用盐酸完全溶解,放出标准状况下5.6L气体,然后再滴入2mol/LNaOH溶液,请回答:
(1)求该混合物中Mg、Al的物质的量?(写计算过程)
(2)若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V= ml。
(3)若该Mg、Al混合物溶于200ml 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为 ml。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第四次摸底考试化学试卷(解析版) 题型:推断题
Ⅱ.选修5——有机化学基础
常用药——羟苯水杨胺,其合成路线如下。回答下列问题:
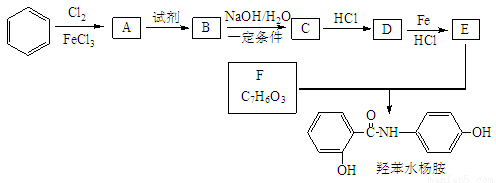
已知:

(1)羟苯水杨胺的化学式为 。对于羟苯水杨胺,下列说法正确的是______。
A.1 mol羟苯水杨胺最多可以和2 mol NaOH反应
B.不能发生硝化反应
C.可发生水解反应
D.可与溴发生取代反应
(2)D的名称为 。
(3)A→B所需试剂为 ;D→E反应的有机反应类型是 。
(4)B→C反应的化学方程式为 。
(5)F存在多种同分异构体。
①F的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是 。
A.质谱仪 B.红外光谱仪 C.元素分析仪 D.核磁共振仪
②F的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应的物质共有 种;
写出其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com