
| A�� | ���յõ���ɫ��������ɫ��Һ | |
| B�� | ���յõ��İ�ɫ�����ǵ����ʵ��������ֻ�����Ļ���� | |
| C�� | ��Ϲ����У��ݳ���ɫ���� | |
| D�� | �����յõ�����Һ�У�c��Cu2+��=0.01 mol•L-1 |
���� 100mL 0.10mol•L-1�� AgNO3��aq����n��AgNO3��=0.1L��0.10mol/L=0.01mol��BaCl2�����ʵ���Ϊ��n��BaCl2��=$\frac{2.08g}{208g/mol}$=0.01mol��CuSO4•5H2O�����ʵ���Ϊ��n��CuSO4•5H2O��=$\frac{2.50g}{250g/mol}$=0.01mol����Ϸ�ӦAg++Cl-�TAgCl����Ba2++SO42-�TBaSO4�����з������
��� �⣺AgNO3�����ʵ���Ϊ��0.1L��0.10mol/L=0.01mol��BaCl2�����ʵ���Ϊ��$\frac{2.08g}{208g/mol}$=0.01mol��CuSO4•5H2O�����ʵ���Ϊ��$\frac{2.50g}{250g/mol}$=0.01mol��
Ag++Cl-�TAgCl��
0.01 0.01 0.01
Ba2++SO4 2-�TBaSO4��
0.01 0.01 0.01
A����ͭ����û�вμӷ�Ӧ�������յõ���ɫ��������ɫ��Һ����A����
B���ɼ����֪���Ȼ��������ʵ���Ϊ0.01mol�����ᱵ��ɫ���������ʵ�������0.01mol����B��ȷ��
C����Ϲ����У�û���������ɣ������ݳ���ɫ���壬��C����
D�������յõ�����Һ�У�Cu2+�����ʵ���Ũ��Ϊ��$\frac{0.01mol}{0.3L}$=0.033mol/L����D����
��ѡB��
���� ���⿼�黯ѧ����ʽ�ļ��㣬��ȷ�μӷ�Ӧ�����ӵ����ʵ��������ʵ����Ĺ�ϵ���������ӷ�Ӧ����ʽ�������ǽ��Ĺؼ����ѶȲ���


 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��DCH3CHCl2��CH2ClCH2Cl��ECH2BrCH2Br��FCH3CHBr2��G
��DCH3CHCl2��CH2ClCH2Cl��ECH2BrCH2Br��FCH3CHBr2��G ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ӧ�� | ��ѧ����ʽ | ��Ӧ���� |
| �ں͢� | ||
| ���͢� | ||
| �͢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ-890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ•mol-1 | |
| B�� | S��g��+O2��g���TSO2��g����H1 S��s��+O2��g���TSO2��g����H2���H1����H2 | |
| C�� | ��֪C��ʯī��s���TC�����ʯ��s����H��0������ʯ��ʯī�ȶ� | |
| D�� | ��֪�к���Ϊ��H=-57.3kJ•mol-1����ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��CH3COOH��aq��+NaOH��aq���TCH3COONa��aq��+H2O��l����H=-57.3 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2 | B�� | KMnO4 | C�� | MgO | D�� | H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 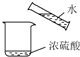 ϡ��Ũ���� | B�� | 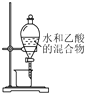 ����ˮ������ | C�� | 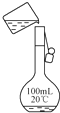 ת����Һ | D�� | 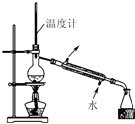 ��ȡ����ˮ ��ȡ����ˮ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com