
| A. | 油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
分析 A.油脂为高级脂肪酸甘油酯;
B.加热生成CuO,立即插入无水乙醇中,乙醇被CuO氧化;
C.化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化;
D.聚酯纤维属于有机物.
解答 解:A.油脂为高级脂肪酸甘油酯,水解生成甘油和高级脂肪酸,而乙酸乙酯水解生成乙醇和乙酸,故A错误;
B.加热生成CuO,立即插入无水乙醇中,乙醇被CuO氧化,则CuO被还原为Cu,铜丝恢复成原来的红色,故B正确;
C.煤的气化是将固体煤中有机质转变为含有CO、H2、CH4等可燃气体;煤的液化指固体煤经化学加工转化成烃类液体燃料和化工原料的过程;两者都生成了新物质,故C错误;
D.制作航天服的聚酯纤维属于有机物,不属于新型无机非金属材料,故D错误.
故选B.
点评 本题主要考查了物质的性质与用途,掌握物质的性质是解题的关键,难度中等.


科目:高中化学 来源: 题型:填空题
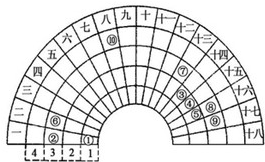 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ①②⑤ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20mL3 mol/L的X溶液 | B. | 20℃30mL2 mol/L的X溶液 | ||
| C. | 20℃10mL4 mol/L的X溶液 | D. | 10℃20mL2 mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
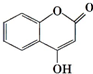 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: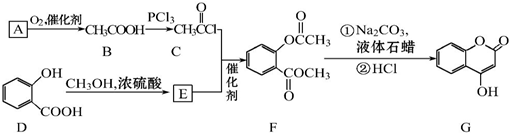
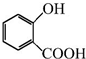 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$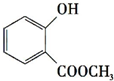 +H2O.
+H2O.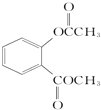 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 反应物总能量小于生成物总能量 | |
| C. | 升高温度,反应速率加快,但反应的△H不变 | |
| D. | 若在原电池中进行,反应放出的热量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
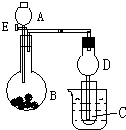 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com