
| 混合物 | 试剂 | 分离方法 | |
| ① | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
| ② | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| ③ | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| ④ | 乙炔(硫化氢) | 硫酸铜 | 洗气 |
| A. | ②③④ | B. | ②③ | C. | ③④ | D. | ③ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
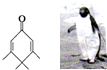 如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )| A. | 若与Penguinone互为同分异构体的酚类且苯环上只有两个取代基的有机物有9种 | |
| B. | Penguinone分子中所有碳原子可能处于同一平面 | |
| C. | Penguinone分子中无酚羟基所以不能使酸性高锰酸钾溶液褪色 | |
| D. | Penguinone分子式为C10H14O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油分馏所得的馏分仍是混合物 | |
| B. | 天然气的主要成分是甲烷、乙烯等气体 | |
| C. | 煤焦油经分馏可得苯和甲苯 | |
| D. | 含C20以上的重油经催化裂化可得汽油、柴油等轻质油 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO2发生了氧化反应 | |
| B. | MnOOH中Mn元素的化合价为+3 | |
| C. | 反应消耗 0.65g Zn,有0.01 mol电子发生转移 | |
| D. | 碱性锌锰电池是一种高效、环境友好的发电装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com