
| A. | 利用澄清石灰水可以鉴别Na2CO3和NaHCO3 | |
| B. | 利用激光笔可以检验豆浆是否属于胶体 | |
| C. | 实验室可以用石英坩埚加热固体NaOH | |
| D. | 用托盘天平称取5.85g NaCl到100mL容量瓶,再用适量蒸馏水溶解定容可配制1.0mol/L NaCl溶液 |
分析 A.澄清石灰水与Na2CO3溶液和NaHCO3溶液反应均生成白色沉淀;
B.豆浆是胶体;
C.石英的成分是二氧化硅;
D.托盘天平称量时只能准确到小数点后一位数.
解答 解:A.澄清石灰水与Na2CO3溶液和NaHCO3溶液反应均生成白色沉淀,现象相同,不能鉴别,故A错误;
B.豆浆是胶体,有丁达尔效应,可检验,故B正确;
C.石英的成分是二氧化硅,在加热条件下与NaOH反应而使坩埚炸裂,故C错误;
D.托盘天平称量时只能准确到小数点后一位数,所以只能称量5.9g药品,不能称量5.85gNaCl,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重元素化合物知识、物质鉴别及反应现象的考查,题目难度不大.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中有CO32- | |
| B. | 向某溶液中加石蕊试液,溶液变红,则原溶液中溶质是酸 | |
| C. | 向某溶液中加氢氧化钠溶液,生成蓝色沉淀,则原溶液中有Cu2+ | |
| D. | 向某溶液中加氯化钡溶液,生成白色沉淀,再加盐酸沉淀不溶解,则原溶液中有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12g C和32g O2所具有的总能量大于44g CO2所具有的总能量 | |
| B. | 12g C所具有的能量一定高于28g CO所具有的能量 | |
| C. | 56g CO和32g O2所具有的总能量大于88gCO2所具有的总能量 | |
| D. | 将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量:④<①<③<② | B. | 密度:①<④<③<② | ||
| C. | 体积:④<①<②<③ | D. | 氢原子数:②<④<③<① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
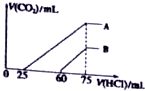 向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的 CO2后,再稀释到100mL.
向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的 CO2后,再稀释到100mL.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
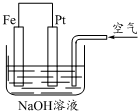 下列有关如图所示装置的叙述中错误的是( )
下列有关如图所示装置的叙述中错误的是( )| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -1648.7 kJ.mo1-1 | B. | -1255.3 kJ.mol-1 | ||
| C. | -861.7 kJ.mol-l | D. | +867.1 kJ.mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com