
 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、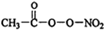 (PAN)等二次污染物.
(PAN)等二次污染物.| m |
| n |
| 5+4-1 |
| 2 |
| 5-1×4-1 |
| 2 |
| 5+1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
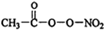 中共有11个共价键,所以1mol PAN中含有的σ键数目为10mol;根据元素周期律,以及第ⅤA族比同周期的ⅥA族第一电离能高,可知N、O、C、H的第一电离能依次减小,
中共有11个共价键,所以1mol PAN中含有的σ键数目为10mol;根据元素周期律,以及第ⅤA族比同周期的ⅥA族第一电离能高,可知N、O、C、H的第一电离能依次减小,| 5+4-1 |
| 2 |
| 5-1×4-1 |
| 2 |
| 5+1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| n |
| 12 |
| 4 |


科目:高中化学 来源: 题型:
 如图,在盛有H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A、外电路的电流方向为:X→外电路→Y |
| B、若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe |
| C、X极上发生的是还原反应,Y极上发生的是氧化反应 |
| D、溶液中氢离子向Y极移动,硫酸根向X极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |

| 实验编号 | 窗口体积/L | 温度/℃ |
| ① | 1.0 | 1200 |
| ② | 2.0 | 1200 |
| ③ | 2.0 | 1300 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 电离能/(kJ?mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
 ,每个COCl2分子内含有
,每个COCl2分子内含有查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当容器内的压强不再变化,可以判断反应已经达到平衡 |
| B、往容器中通入稀有气体He,由于压强增大,所以反应速率增大 |
| C、往容器中加入少量A,反应速率增大 |
| D、若反应是放热反应,升高温度,正反应速率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com