
����Ŀ��5�ֹ�������A��B��C��D��E�ɱ��в�ͬ������������ɣ����Ǿ�������ˮ��
������ | Na+�� Al3+Fe3+�� Cu2+��Ba2+ |
������ | OH����Cl����CO32����NO3����SO4�� |
�ֱ�ȡ���ǵ�ˮ��Һ����ʵ�飬������£���A��Һ��C��Һ��Ϻ������ɫ��������ó����м�������ϡHNO3 �� ���������ܽ⣬ʣ���ɫ���壻��B��Һ��E��Һ��Ϻ�������ɫ������ͬʱ�����������壻
������C��Һ��D��Һ��Ϻ������ɫ����������C��Һ��D��Һ��Ϻ�������
��B��Һ��D��Һ��Ϻ�������
�ݽ�38.4g CuƬͶ��װ������D��Һ���Թ��У�CuƬ���ܽ⣬�ٵμ�1.6molL��1ϡH2SO4 �� Cu���ܽ⣬�ܿڸ����к���ɫ������֣�
��1���ݴ��ƶ�A��C�Ļ�ѧʽΪ��A��C ��
��2��д��������з�����Ӧ�Ļ�ѧ����ʽ ��
��3��D��Һ�е���ʯ����Һ�������� �� ԭ�����������ӷ���ʽ˵������
��4�����������Ҫ��CuƬ��ȫ�ܽ⣬���ټ���ϡH2SO4�������mL��
��5������500mL 3molL��1��E��Һ�������11.2L CO2���壨��״�� �£�����Ӧ����Һ�и����ӵ�������Ũ����С�����˳��Ϊ ��
��6�����ö��Ե缫���A��B�Ļ����Һ�����ʵ����ʵ�����Ϊ0.1mol����������ϵ�л���ͨ�����������������������״���£�V��ͨ�����ӵ����ʵ���n�Ĺ�ϵ����������������ˮ����
���𰸡�
��1��CuSO4,Ba��OH��2
��2��2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2��
��3������ɫ��ɺ�ɫ,Al3++3H2O?Al��OH��3+3H+
��4��500
��5��c��H+����c��OH������c��CO32������c��HCO3������c��Na+��
��6��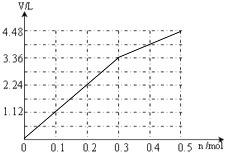
���������⣺��1�����ƶ�A��C�Ļ�ѧʽΪCuSO4��Ba��OH��2 ��
���Դ��ǣ�CuSO4��Ba��OH��2��
��2������ڣ�EΪNa2CO3��Һ��BΪFeCl3��Һ�����߷���˫ˮ�ⷴӦ�����������������Ͷ�����̼�����䷴Ӧ����ʽΪ��2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2����
���Դ��ǣ�2Fe3++3CO32��+3H2O=2Fe��OH��3��+3CO2����
��3��DΪAl��NO3��3��Һ��������Һ�����ԣ���Ϊ������ˮ�����������ӣ��� Al3++3H2OAl��OH��3+3H+����������Һ�е���ʯ����Һ����Һ������ɫ��ɺ�ɫ��
���Դ��ǣ�����ɫ��ɺ�ɫ�� Al3++3H2OAl��OH��3+3H+��
��4��38.4 g Cu�����ʵ���Ϊ�� ![]() =0.6mol��������з��������ӷ�Ӧ����ʽΪ��3Cu+8H++2NO3��=3Cu2++2NO+4H2O����Ҫ��CuƬ��ȫ�ܽ⣬��Ҫ�����ӵ����ʵ���Ϊ1.6mol�������ټ���ϡH2SO4�������ΪV����1.6mol/L��V��2=1.6mol����V=500mL��
=0.6mol��������з��������ӷ�Ӧ����ʽΪ��3Cu+8H++2NO3��=3Cu2++2NO+4H2O����Ҫ��CuƬ��ȫ�ܽ⣬��Ҫ�����ӵ����ʵ���Ϊ1.6mol�������ټ���ϡH2SO4�������ΪV����1.6mol/L��V��2=1.6mol����V=500mL��
���Դ��ǣ�500��
��5��500mL 3molL��1��Na2CO3��Һ�е�Na2CO3���ʵ���=0.5L��3mol/L=1.5mol��11.2L CO2�����ʵ���= ![]() =0.5mol��������ӦNa2CO3+CO2+H2O=2NaHCO3���ɷ���ʽ��֪������1molNaHCO3��ʣ��1molNa2CO3����Һ��������Ũ�����̼�������̼�����ˮ�⣬��Һ�ʼ��ԣ�̼�������ˮ��̶�С��̼���ˮ��̶ȣ�����Һ������Ũ�ȣ�c��H+����c��OH������c��CO32������c��HCO3������c��Na+����
=0.5mol��������ӦNa2CO3+CO2+H2O=2NaHCO3���ɷ���ʽ��֪������1molNaHCO3��ʣ��1molNa2CO3����Һ��������Ũ�����̼�������̼�����ˮ�⣬��Һ�ʼ��ԣ�̼�������ˮ��̶�С��̼���ˮ��̶ȣ�����Һ������Ũ�ȣ�c��H+����c��OH������c��CO32������c��HCO3������c��Na+����
���Դ��ǣ�c��H+����c��OH������c��CO32������c��HCO3������c��Na+����
��6�����ö��Ե缫���CuSO4��FeCl3�Ļ����Һ�����ʵ����ʵ�����Ϊ0.1mol��
���ȣ�����������Ӧ��2Cl����2e��=Cl2������n�����ӣ�= ![]() ��2=
��2= ![]() ����V=11.2n��������ԭ���غ��֪������������������=
����V=11.2n��������ԭ���غ��֪������������������= ![]() ��22.4L/mol=3.36L����ʱת�Ƶ������ʵ���Ϊ0.3mol��
��22.4L/mol=3.36L����ʱת�Ƶ������ʵ���Ϊ0.3mol��
Ȼ������������Ӧ��4OH����4e��=O2��+2H2O����n�����ӣ�= ![]() ��4=����V=5.6n��
��4=����V=5.6n��
��ͨ�����������������������״���£�V��ͨ�����ӵ����ʵ���n�Ĺ�ϵΪ�� 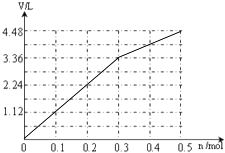 ��
��
���Դ��ǣ�  ��
��


 һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д� ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������100mL��Cu2+��Al3+��NH4+��H+��Cl������Һ�������Һ����μ���2.5mol/LNaOH��Һ������NaOH ��Һ�������mL����������������ʵ�����mol����ϵ����ͼ��ʾ��

��1��B��ij�����Ļ�ѧʽΪ______________��
��2��ԭ��Һ��Cu2+�����ʵ���Ϊ______��ԭ��Һ��Cl�����ʵ���Ũ��Ϊ________��x-y=__________��
����A��B��C��DΪ��ѧ���������Ҿ�����ͬһ��Ԫ�أ��ת����ϵ��ͼ(��Ӧ���������������Ѿ���ȥ)��
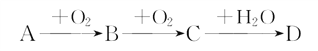
��1����A��ˮ��Һ��ʹʪ��ĺ�ɫʯ����ֽ������D��ϡ��Һ��ʹʪ�����ɫʯ����ֽ��졣��D�Ļ�ѧʽΪ___________��
��2����AΪ���ʣ�DΪǿ�������Ԫ�ص�ԭ���������ӵ���ĿС��18��д��C��D�Ļ�ѧ����ʽ��_____________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϊ�з��ϰ�ȫҪ�����
A. ����ú��ʹ�û������
B. �����ڼ䣬�ڿ����Ĺ㳡ȼ���̻�����
C. �õ�ȼ�Ļ����Һ������ƿ�ڼ����Ƿ�©��
D. ʵ��ʱ����ˮ����Ũ��������ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Һ����������������������Һ ���Ҵ��Ͷ��� ���廯�ƺ͵������ˮ��Һ���������ϸ����Һ����ȷ���������ǣ� ��
A.��Һ ���� ��ȡ
B.��ȡ ���� ��Һ
C.��Һ ��ȡ ����
D.���� ��ȡ ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��Ӧԭ�����������������
��1����֪����CO��g��+2H2��g��CH3OH��g����Hl=��91kJmol��l
��2CH3OH��g��CH3OCH3��g��+H2O��g����H2=��24kJmol��l
��CO��g��+H2O��g��CO2��g��+H2��g����H3=��41kJmol��l
��������Ӧ��ƽ�ⳣ������ΪK1��K2��K3
��Ӧ 3CO��g��+3H2��g��CH3OCH3��g��+CO2��g����H= ��
��ѧƽ�ⳣ��K=���ú�K1��K2��K3�Ĵ���ʽ��ʾ����
��2��һ�������£����������Ϊ1��2��CO��H2����ͨ�����һ�����ܱ������з�����Ӧ3CO��g��+3H2��g��CH3OCH3��g��+CO2��g����������˵����Ӧ�ﵽƽ��״̬�� ��
a����ϵѹǿ���ֲ���
b����������ܶȱ��ֲ���
c��CO��H2�����ʵ������ֲ���
d��CO�������ٶȵ���CO2����������
��3����ѧ�ҷ�����ʹNH3ֱ������ȼ�ϵ�صķ�������װ���ò������缫������������Һ�У�һ���缫ͨ���������һ�缫ͨ��NH3 �� ���ط�ӦʽΪ��4NH3+3O2=2N2+6H2O���������ҺӦ��������ԡ��������ԡ��������ԡ�����д�������ĵ缫��Ӧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3���Լױ���ϩ�������E����һ�����ںϳɿ�Ѫ˨ҩ���м��壬��ϳ�·�����£� 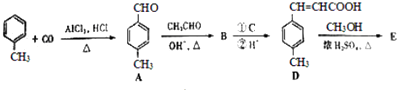
��֪��HCHO+CH3CHO ![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
��1����FeCl3��Һ����ɫ�ұ�����������ȡ������A��ͬ���칹�����֣�B�к��������ŵ�����Ϊ ��
��2���Լ�C��ѡ�������е� ��
a����ˮ
b��������Һ
c������KMnO4��Һ
d������Cu��OH��2����Һ
��3��![]() ��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ ��
��E��һ��ͬ���칹�壬������������NaOH��Һ���ȵĻ�ѧ����ʽΪ ��
��4��E��һ�������¿������ɸ߾���F��F�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ�������
A.������̼����Ԫ�ص�����������ͬ����Ϊͬϵ��
B.CH2�TCH2��CH2�TCH��CH�TCH2��Ϊͬϵ��
C.![]() ��
�� ![]() ��Ϊͬ���칹��
��Ϊͬ���칹��
D.ͬ���칹��Ļ�ѧ���ʿ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com