
| A. | 第三列为ⅠB | B. | 第十三列为ⅢA | C. | 第十六列为ⅣA | D. | 第十八列为0A |
分析 根据族与列的对应关系解答,族与列的关系如表:
| 列数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 族 | ⅠA | ⅡA | ⅢB | ⅣB | ⅤB | ⅥB | ⅦB | Ⅷ | ⅠB | ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||
解答 解:族与列的关系如表:
| 列数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 族 | ⅠA | ⅡA | ⅢB | ⅣB | ⅤB | ⅥB | ⅦB | Ⅷ | ⅠB | ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||
点评 本题考查元素周期表的结构,难度不大,旨在考查学生对周期表的整体把握,注意基础知识的掌握.


科目:高中化学 来源: 题型:选择题
| KCl | K2SO4 | ZnSO4 | ZnCl2 | |
| (1) | 0.3mol | 0.2mol | 0.1mol | - |
| (2) | 0.1mol | 0.3mol | - | 0.2mol |
| A. | Cl-的物质的量相同 | B. | SO42-的数目相同 | ||
| C. | K+的数目相同 | D. | Zn2+的物质的量不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
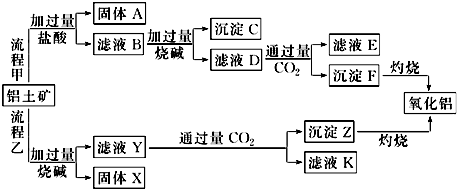
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的原子数目为NA.
的原子数目为NA.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述II |
| A | SO2有氧化性 | SO2能使酸性KMnO4溶液褪色 |
| B | SiO2导电能力强 | 可用于制造通讯光缆 |
| C | Al有还原性,在某些反应中热效应大 | 利用铝热反应冶炼金属Mn |
| D | 常温下铁与浓硫酸、浓硝酸均不反应 | 可用铁槽车密封运送浓硫酸、浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
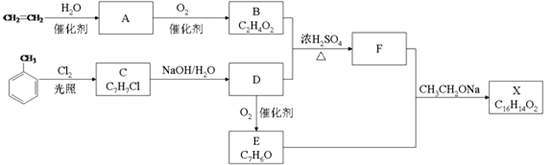
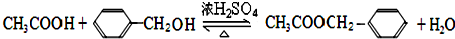 .
. .
.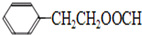 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
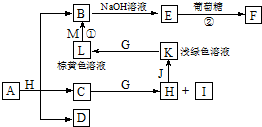 各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.
各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
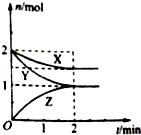 在容积固定的2L密闭容器中,一定条件下发生如下反应:X(g)+2Y(g)?nZ(g),反应过程中各物质的量与时间的关系如图所示.完成下列填空:
在容积固定的2L密闭容器中,一定条件下发生如下反应:X(g)+2Y(g)?nZ(g),反应过程中各物质的量与时间的关系如图所示.完成下列填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com