
N2(g)+3H2(g) 2NH3(g) △H<0,当反应达到平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,当反应达到平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压
A.③④ B.①② C.②③ D.①④
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高一上第二次月考化学试卷(解析版) 题型:选择题
下列反应中,可用离子方程式H++OH- = H2O表示的是 ( )
A.CH3COOH+NaOH = CH3COONa+H2O
B.H2SO4+Ba(OH)2 = BaSO4↓+2H2O
C.HNO3+KOH = KNO3+H2O
D.2HCl+Cu(OH)2 = CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源:2016届贵州市高三上学期第五次月考理综化学试卷(解析版) 题型:实验题
中国沿海某城市采用反渗透法将海水淡化,得到淡水供市民使用,剩余母液继续加工获得其他产品。母液中主要含有Cl-、Na+、K+、Ca2+、SO42-、Br-等离子。某实验小组同学模拟工业生产流程,进行如下实验.

(1)写出实验室制备氯气的化学方程式_____________________;
(2)海水淡化的方法还有____________(写出一种);
(3)I中,电解饱和食盐水的工业生产叫做氯碱工业,写出该反应的离子方程式__________;
(4)Cl2和Br2均为双原子分子,从原子结构的角度解释其原因_____________________;
(5)Ⅲ中,加入适量CaCl2固体的目的是_____________________;
(6)写出IV中反应的离子方程式_____________________;
(7)与过程II类似,工业上常用“空气吹出法”实现海水提溴,将1m3海水浓缩至1L,使用该法最终得到36g Br2,若提取率为60%,则原海水中溴的浓度为__________ mg/L。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期第五次月考化学试卷(解析版) 题型:选择题
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是:

A.反应开始到10s,用Z表示的反应速率为0.158mol/(L•s)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期12月质检化学试卷(解析版) 题型:推断题
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(1)Z在周期表中的位置是_________________。
(2)X、Y、Q各自形成简单离子,其中离子半径最大的是___________(填离子符号)。
(3)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,则M的氧化物与强碱溶液反应的离子方程式是___________。
(4)Q和R按原子个数比1:1组成的化合物甲,是一种“绿色”氧化剂.
①甲中所含共价键类型是___________。
②空气阴极法电解制备甲的装置如图所示.在碱性溶液中,利用空气中的氧气还原得到甲和稀碱的溶液.图中直流电源的a是_____极,阴极的电极反应式是___________。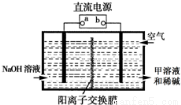
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:选择题
在一密闭容器中,反应aA(g)  bB(g),达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,B的浓度是原平衡的60%,则( )
bB(g),达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡后,B的浓度是原平衡的60%,则( )
A.平衡向正反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数减小了 D. a > b
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
能在溶液中大量共存的一组离子是( )
A.Cu2+、SO42﹣、OH﹣、K+ B.Na+、CO32﹣、H+、Cl﹣
C.H+、Cl﹣、NO3﹣、Ba2+ D.Ca2+、H+、CO32﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:填空题
已知下表为25℃时某些弱酸的电离平衡常数;下图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。
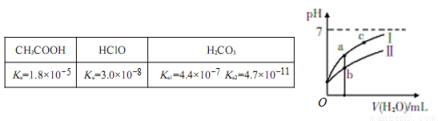
(1)图像中,曲线Ⅰ表示的酸是____(填化学式);
(2)a、b、c三点中,水的电离程度由大到小的顺序是___________(用编号表示)。
(3)25℃时,NaClO溶液的水解平衡常数Kh=_______________。
(4)25℃时,NaHCO3溶液存在水解平衡,写出其水解的离子方程式
(5)0.1mol/L Na2CO3溶液中c(OH-)—c(H+)=_________(用含c(HCO3-)、c(H2CO3)的关系式表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二上期中测试化学试卷(解析版) 题型:选择题
某化学科研小组在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g) cC(g)表示]的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是( )
cC(g)表示]的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是( )
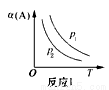



A.反应I:若p1>p2,则此反应只能在高温下自发进行
B.反应Ⅱ:此反应的△H<0,且T1<T2
C.反应Ⅲ:表示t1时刻一定是使用催化剂对反应速率的影响
D.反应Ⅳ:表示t1时刻增大B的浓度对反应速率的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com