
某研究性学习小组在做制乙烯实验中,发现有“刺激性气体产物,且烧瓶中的溶液变黑色”,他们认为可能的气体产物有乙烯、二氧化碳、二氧化硫等.已知:CH3CH═CH2与酸性高锰酸钾溶液反应生成CH3COOH、CO2.

(1)实验室制乙烯实验中,下列错误操作可能引发安全事故的是 .
A.加热温度没有迅速升至170℃
B.忘记加碎瓷片
C.直接加热烧瓶
D.用医用消毒酒精
E.实验完毕,先熄灭酒精灯,后拆导管
(2)中学化学中温度计的作用有:①测定溶液温度,②测定 温度.
(3)甲同学设计如图1及图2所示装置检验该气体产物:方案Ⅰ,不能检验 二 ;方案Ⅱ,能检验 .
(4)乙同学认为制乙烯过程中,可能有CO产生,他在甲同学设计的装置后面连接如图3所示装置,探究是否有一氧化碳生成.
①乙同学应在甲同学设计的 (填“方案Ⅰ”、“方案Ⅱ”或“方案Ⅰ和方案Ⅱ”)的装置后面连接该装置;
②A瓶装的试剂是 ;
③B的硬质试管中装入 ,确认有一氧化碳生成的实验现象是 .
考点:
性质实验方案的设计;乙醇的消去反应.
专题:
实验题.
分析:
(1)根据试验中不加碎瓷片、没有垫石棉网、先熄灭酒精灯等不正确的操作可能引发安全事故来回答;
(2)温度计可测溶液温度和蒸气温度;
(3)根据二氧化碳和二氧化硫的化学性质以及实验现象来回答;
(4)一氧化碳具有还原性,可以将金属氧化物氧化为金属单质,根据实验现象可以确定一氧化碳的生成,注意实验中的干扰因素,结合实验目的和原理来选择装置回答即可.
解答:
解:(1)不加碎瓷片、没有垫石棉网、先熄灭酒精灯等不正确的操作都可能引发安全事故,故答案为:BCE;
(2)温度计可测溶液温度和蒸气温度,如石油蒸馏用温度计测定馏分温度,故答案为:蒸汽;
(3)方案Ⅰ,氢氧化钠溶液能吸收二氧化硫和二氧化碳,且二氧化硫和二氧化碳都能使澄清石灰水变浑浊,所以只能检验二氧化硫、乙烯,不能检验二氧化碳;方案Ⅱ,酸性高锰酸钾溶液能同时与二氧化硫和乙烯反应,故该方案只能检验二氧化硫,不能检验乙烯.根据新信息可知,酸性高锰酸钾溶液能将乙烯氧化成二氧化碳,所以该方案不能检验原气体产物中是否有二氧化碳.
故答案为:二氧化碳;二氧化硫;
(4)①检验原气体中是否有一氧化碳,关键是除去二氧化碳和二氧化硫,并检验二氧化硫和二氧化碳是否除净.方案I的装置有除二氧化碳和二氧化硫装置,并能检验是否除净,乙烯对检验一氧化碳没有影响;方案Ⅱ无检验二氧化碳气体是否除净装置.故答案为:方案Ⅰ;
②A装置用于干燥气体,应装浓硫酸;故答案为:浓硫酸;
③一氧化碳具有还原性,可以将金属氧化物氧化为金属单质,根据实验现象可以确定一氧化碳的生成;B装置中可以装氧化铜或氧化铁;C装置用于检验是否有二氧化碳生成,尾气用气球吸收,若有一氧化碳生成,则可观察到黑色粉末变红色(或红色粉末变黑色),C中澄清石灰水变浑浊.
故答案为:氧化铜(或氧化铁);黑色粉末变红色(或红色粉末变黑色),C中澄清石灰水变浑浊.
点评:
本题是一道实验方案的设计和探究题,考查学生分析和解决问题的能力,难度大,综合性强.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
从柑橘中提取得到结构简式如下图所示的化合物,则下列有关它的推断错误的是( )
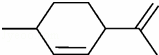
|
| A. | 分子式为C10H16 | B. | 常温下呈固态,比水重 |
|
| C. | 其一氯代物有8种 | D. | 能与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g)═2HF(g)△H=﹣270kJ•mol﹣1,下列说法正确的是( )
|
| A. | 2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 |
|
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
|
| C. | 在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
|
| D. | 1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 焓变等于反应物的总能量减去生成物的总能量 |
|
| B. | 焓变等于反应物的键能总和减去生成物的键能总和 |
|
| C. | 断裂化学键是放热过程 |
|
| D. | 形成新的化学键是吸热过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
| 2011.3.18,实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③SO42﹣向Cu极移动 ④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu﹣→Zn ⑥正极反应式:Cu+2e﹣═Cu2+,发生氧化反应 |
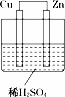
|
| A. | ①②③ | B. | ②④ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题.
| W | X | Y | Z | |
| 结构 或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于 族.
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是 (填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号).
a.自然界中的含量 b.相应氯化物水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因: ,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是 ,混合后溶液中离子浓度由大到小的顺序是 .
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.
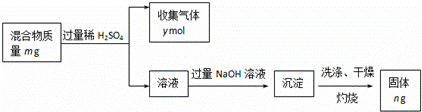
能确定混合物中Y的质量分数的数据有 (填序号).
a.m、n b.m、y c.n、y.
查看答案和解析>>
科目:高中化学 来源: 题型:
如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )
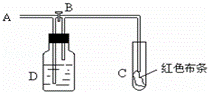
A. D中不可能是浓硫酸 B. 通入的氯气含有水蒸气
C. D中不可能是NaOH溶液 D. D中可以是饱和食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
反应:PCl5(g)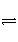
 PCl3(g)+Cl2(g)① 2HI(g)
PCl3(g)+Cl2(g)① 2HI(g)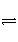
 H2(g)+I2(g)②
H2(g)+I2(g)②
2NO2(g)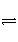
 N2O4(g)③ 在一定条件下,化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
N2O4(g)③ 在一定条件下,化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
A.均不变 B.均增大
C.①增大,②不变,③减小 D.①减小,②不变,③增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com