
下列物质不能溶于浓氨水的是( )
A.AgCl B.Cu(OH)2
C.AgOH D.Fe(OH)3
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
实验证明,多数能自发进行的反应都是放热反应。对此说法的理解正确的是( )
A.所有的放热反应都是自发进行的
B.所有的自发反应都是放热的
C.焓变是影响反应是否具有自发性的一种重要因素
D.焓变是决定反应是否具有自发性的唯一判据
查看答案和解析>>
科目:高中化学 来源: 题型:
在300 ℃时,改变起始反应物中n(H2)对反应N2(g)+3H2(g)2NH3(g) ΔH<0的影响如图所示,下列说法正确的是( )
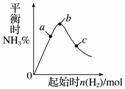
A.反应在b点达到平衡
B.b点H2的转化率最高
C.c点N2的转化率最高
D.a、b、c三点的平衡常数Kb>Ka>Kc
查看答案和解析>>
科目:高中化学 来源: 题型:
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示。
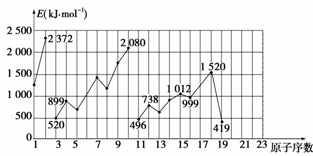
试根据元素在同期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)同主族内不同元素的E值变化的特点是_________________________________。各主
族中E值的这种变化特点体现了元素性质的____________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是________(填写编号,多选倒扣)。
①E(砷)>E(硒) ②E(砷)<E(硒)
③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 mol气态Ca原子失去最外层一个电子所需能量E值的范围:
_____<E<____________。
(4)10号元素E值较大的原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下微粒含配位键的是( )
①N2H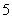 ②CH4 ③OH- ④NH
②CH4 ③OH- ④NH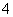 ⑤Fe(CO)3
⑤Fe(CO)3
⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
A.①②④⑦⑧ B.③④⑤⑥⑦
C.①④⑤⑥⑦⑧ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)写出与H2O分子电子数相等的微粒________(写一个即可)。
(2)水分子在特定条件下容易得到一个H+形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是________。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)将白色的无水CuSO4固体溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配合离子。请写出生成此配合离子的离子方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于范德华力的叙述不正确的是( )
A.是一种较弱的化学键
B.范德华力较弱,破坏它所需能量较少
C.范德华力对物质的熔、沸点有影响
D.稀有气体原子之间存在范德华力
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 AB
解析 水分子中各原子已达到稳定结构,H3O+是H+和H2O中的O形成配位键;[B(OH)4]-是3个OH-与B原子形成3个共价键,还有1个OH-的O与B形成配位键;其他项均不能形成配位键。
★ ★★
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的铁和足量的稀硝酸或浓硝酸完全反应,在相同条件下,用排水集气法收集产生的气体。下列叙述一定正确的是( )
①硝酸浓度越大,消耗的硝酸越少
②硝酸浓度不同,生成的Fe(NO3)3的物质的量相同
③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同
A.只有② B.②④ C.③④ D.①②③
★ ★★
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com