
| A�� | c��NaOH����c��NH3•H2O�� | |
| B�� | c��Na+��=c��NH4+�� | |
| C�� | �������NaOH��NH3•H2O��Һ�ֱ���������Si��ȫ��Ӧ��NH3•H2O������H2�� | |
| D�� | ����ͬŨ�ȵ�������Һ�ֱ���������NaOH��NH3•H2O��Һǡ�÷�Ӧ��ȫ��NaOH���ĵ�������Һ����� |
���� A��һˮ�ϰ�Ϊ���������Һ�д��ڵ���ƽ�⣻
B��pH��ȵ�NaOH��NH3•H2O��Һ������������Ũ����ͬ��笠����Ӻ�������Ũ����ͬ��
C�����һˮ�ϰ���Һ����Ӧ��
D��pH��ȵ�NaOH��NH3•H2O��Һ������������Ũ����ͬ���������ᷴӦ��һˮ�ϰ��ֵ�������������ӣ�
��� �⣺A��pH��ȵ�NaOH��NH3•H2O��Һ�У�һˮ�ϰ���֪����ƽ�⣬�����ṩ��ͬ����������Ũ�ȣ�һˮ�ϰ���ҺŨ�ȴ�c��NaOH����c��NH3•H2O����A����
B��pH��ȵ�NaOH��NH3•H2O��Һ������������Ũ����ͬ��笠����Ӻ�������Ũ����ͬ��c��Na+��=c��NH4+������B��ȷ��
C�����һˮ�ϰ���Һ����Ӧ���������NaOH��NH3•H2O��Һ�ֱ���������Si��ȫ��Ӧ������������Һ������H2�࣬��C����
D��pH��ȵ�NaOH��NH3•H2O��Һ������������Ũ����ͬ���������ᷴӦ��һˮ�ϰ��ֵ�������������ӣ�NH3•H2O��Һ��������������Һ�࣬��D����
��ѡB��
���� ���⿼����������ʵ���ƽ���Ӱ�����ء���ҺPH�ļ�������жϣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
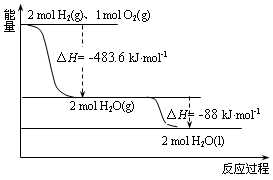
| A�� | ������ȼ���ȡ�H=-241.8 kJ•mol-1 | |
| B�� | 2 mol H2��g����1 mol O2��g���������������2 mol H2O��g�� ������������� | |
| C�� | Һ̬ˮ�ֽ���Ȼ�ѧ����ʽΪ��2H2O��l��=2H2��g��+O2��g����H=+571.6 kJ•mol-1 | |
| D�� | H2O��g������H2O��l��ʱ���ϼ����յ�����С�ڳɼ��ų������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4L��O2����NO2��ɵĻ�����庬�е�ԭ����Ϊ2NA | |
| B�� | 1mol�ǻ���1mol���������Ӻ��еĵ�������Ϊ9NA | |
| C�� | 0.1molFe2+������H2O2��Һ��Ӧ��ת�Ƶĵ�����Ϊ0.1NA | |
| D�� | 1L1 mol•L-1NaF��Һ�к���F-����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
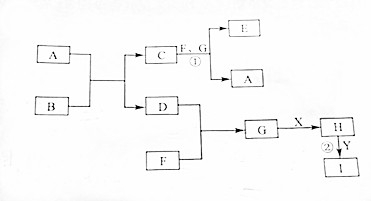 �й����ʵ�ת����ϵ��ͼ��ʾ��������������������ȥ��������A��D��F��GΪ���������壬DΪ���ʣ�A��F��GΪ�����GΪ�غ�ɫ��BΪ����ɫ���壮X�������Һ�壬Y�dz����Ľ������ʣ�I��ҺΪ��ɫ��
�й����ʵ�ת����ϵ��ͼ��ʾ��������������������ȥ��������A��D��F��GΪ���������壬DΪ���ʣ�A��F��GΪ�����GΪ�غ�ɫ��BΪ����ɫ���壮X�������Һ�壬Y�dz����Ľ������ʣ�I��ҺΪ��ɫ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ı��¶ȣ���������NaClO3�����ʵ������ʱ�����������ӷ�ӦΪ��3Cl2+6OH-$\frac{\underline{\;\;��\;\;}}{\;}$5Cl-+ClO3-+3H2O | |
| B�� | ij�¶��£���Ӧ������Һ��c��ClO-����c��ClO3-��=1��2�����������ӷ�ӦΪ��7Cl2+14OH-$\frac{\underline{\;\;��\;\;}}{\;}$11Cl-+ClO-+2ClO3-+7H2O | |
| C�� | �μӷ�Ӧ��Cl2��NaOH�����ʵ����Ĺ�ϵһ����a=0.5b | |
| D�� | �ı��¶ȣ���Ӧ��ת�Ƶ��ӵ����ʵ�������Ϊb mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƹ�ʹ��ȼú������������SO2��Ⱦ | |
| B�� | �Ӵ�ʯ�͡�ú̿�Ŀ����ٶȣ����ӻ�ʯȼ�ϵĹ�Ӧ�� | |
| C�� | ���ƿ���ȼ�ϵ������������������β����Ⱦ | |
| D�� | ʵʩ�̻����̣������ﳾ��Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��CCl4�������ˮ����ȡ���� | |
| B�� | ��ij��ɫ��Һ�м���������������ɫ������֤����Һ�к���Cl- | |
| C�� | ���ü��ȵķ�����ȥ�Ȼ��ƹ����л��е��Ȼ�粒��� | |
| D�� | �ö����ЧӦ������۽����ʳ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��ͬѹ�£�������ͬ���������������壬ռ����ͬ����� | |
| B�� | ͬ��ͬѹ�£���ͬ���ʵ����������κ����壬������ͬ�ķ����� | |
| C�� | ͬ��ͬѹ�£���ͬ������������壬���ʵ�����ͬ | |
| D�� | ͬ��ͬѹ�£�2��O2��2����CO2��CO��ɵĻ�����庬����ͬ��ԭ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com