
关于 Na2CO3和NaHCO3下列说法不正确的是( )
A. 可以用加热的方法除去Na2CO3中的NaHCO3
B. 分别向Na2CO3和NaHCO3溶液滴加少量盐酸,产生CO2气体较快的为NaHCO3
C. 可以用Ca(OH)2溶液区分Na2CO3和NaHCO3溶液
D. Na2CO3比NaHCO3易溶于水
考点: 钠的重要化合物.
分析: A.加热Na2CO3不分解,加热NaHCO3分解产生碳酸钠、水和二氧化碳气体;
B.NaHCO3与盐酸反应快;
C.加入澄清的石灰水,Na2CO3溶液和NaHCO3溶液都能生成沉淀;
D.相同的温度下,NaHCO3溶解度比Na2CO3小.
解答: 解:A.加热Na2CO3不分解,加热NaHCO3分解产生碳酸钠、水和二氧化碳气体,所以可以用加热的方法除去Na2CO3中的NaHCO3,故A正确;
B.NaHCO3与盐酸反应快,所以分别向Na2CO3和NaHCO3溶液滴加少量盐酸,产生CO2气体较快的为NaHCO3,故B正确;
C.加入澄清的石灰水,Na2CO3溶液和NaHCO3溶液都能生成CaCO3沉淀,不能区别两种溶液,故C错误;
D.相同的温度下,NaHCO3溶解度比Na2CO3小,所以Na2CO3比NaHCO3易溶于水,故D正确.
故选C.
点评: 本题考查Na2CO3和NaHCO3的性质,题目难度不大,本题侧重于二者性质区别的考查,注意与澄清石灰水反应的性质.


科目:高中化学 来源: 题型:
一定质量的某有机物和足量钠反应,可得VaL气体,等质量的该有机物如果与足量小苏打反应,同温同压得到VbL气体,若Va=Vb,则该有机物可能是( )
|
| A. | HOCH2COOH | B. | HO﹣CH2CH2﹣CHO |
|
| C. | HOOC﹣COOH | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )
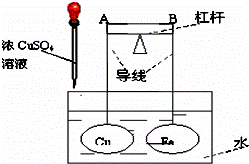
A. 杠杆为导体或绝缘体时,均为A端高B端低
B. 杠杆为导体或绝缘体时,均为A端低B端高
C. 当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D. 当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A. 苏打溶液与稀盐酸反应的离子反应方程式:HCO3﹣+H+═CO2↑+H2O
B. Fe2O3与HI:Fe2O3+6H+═2Fe3++3H2O
C. NaHCO3溶液中滴加少量澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣
D. 浓烧碱溶液中加入铝片:Al+OH﹣+H2O═AlO2﹣+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某芳香族化合物A式量小于150,氢氧质量比为1:8,完全燃烧后只生成CO2和H2O.取等质量的A分别与足量NaHCO3和Na反应,生成的气体在同温同压下的体积比为1:1.工业常用A来合成药物B及医药中间体G,流程如下:
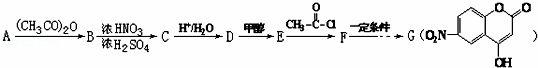
已知:
①CH3CH2OH CH3COOCHCH2CH3
CH3COOCHCH2CH3
②
(1)写出A含有的官能团的名称 ,D的结构简式 .
(2)D生成E的反应类型是 .
(3)写出F与过量NaOH共热时反应的化学方程式: .
(4)A自身之间也能发生缩聚反应,写出该高分子聚合物的化学式.
(5)B有多种同分异构体,写出符合下列条件的一种物质的结构简式 或 .
①只有一种官能团 ②苯环上的一氯取代物只有二种
③能发生银镜反应 ④核磁共振谱共有四组峰,峰的面积比为3:2:2:1
(6)下列有关说法正确的是 .
A.可由A经一步反应获得D;
B. 与G互为同分异构体
与G互为同分异构体
C.G易水解,可用FeCl3溶液检验是否发生水解
D.1molG一定能和5mol氢气反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1gH2燃烧生成液态水时放出142.9kJ的热量,以下热化学方程式正确的是( )
|
| A. | 2H2(g)+O2(g)=2H2O(l)△H=﹣142.9kJ•mol﹣1 |
|
| B. | 2H2(g)+O2(g)=2H2O(l)△H=+571.6kJ•mol﹣1 |
|
| C. | 2H2+O2=2H2O△H=﹣571.6kJ•mol﹣1 |
|
| D. | H2(g)+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65KJ的热量.
(1)写出该反应的热化学方程式 .
(2)已知H2O(l)═H2O(g);△H=+44kJ•mol﹣1,则16g液态水气化时,放出的热量是 KJ.
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温恒容的容器中进行反应 A(g)⇌2B(g)+C(g);△H>0,若反应物浓度由0.1mol•L﹣1降到0.06mol•L﹣1需20s,那么由0.06mol•L﹣1降到0.024mol•L﹣1,需反应的时间为( )
|
| A. | 等于18s | B. | 等于12s | C. | 大于18s | D. | 小于18s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com