
·ÖĪö £Ø1£©¼ī»ņĒæ¼īČõĖįŃĪĘäČÜŅŗ¶¼³Ź¼īŠŌ£»
£Ø2£©pH=-lgc£ØH+£©£»“×ĖįÄĘ“Ł½ųĖ®µēĄė£¬øł¾ŻĒāĄė×ÓÅØ¶Č½įŗĻĖ®µÄĄė×Ó»ż³£Źż¼ĘĖćĒāŃõøłĄė×ÓÅØ¶Č£»“×ĖįøłĄė×ÓŌŚČÜŅŗÖŠĖ®½āÉś³ÉĒāŃõøłĄė×Ó£¬ČÜŅŗĻŌ¼īŠŌ£»
£Ø3£©“×ĖįŹĒČõµē½āÖŹ£¬ĀČ»ÆĒāŹĒĒæµē½āÖŹ£¬“×Ėį“ęŌŚµēĄėĘ½ŗā£¬ĀČ»ÆĒā²»“ęŌŚµēĄėĘ½ŗā£¬½«µČpHµÄ“×ĖįŗĶŃĪĖįĻ”ŹĶŗóČÜŅŗµÄpHČŌČ»ĻąµČ£¬Ōņ“×ĖįĻ”ŹĶµÄ±¶Źż“óÓŚŃĪĖį£®
½ā“š ½ā£ŗ£Ø1£©¼ī»ņĒæ¼īČõĖįŃĪĘäČÜŅŗ¶¼³Ź¼īŠŌ£¬ĒāŃõ»ÆÄĘŗĶ°±Ė®”¢“×ĖįÄĘČÜŅŗ¶¼³Ź¼īŠŌ£¬
¹Ź“š°øĪŖ£ŗ¢Ś¢Ü¢Ż£»
£Ø2£©³£ĪĀĻĀ0.01mol/L HClČÜŅŗµÄpH=-lgc£ØH+£©=-lg0.01=2£¬0.01mol/L NaOHČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČ0.01mol/L£¬Ōņc£ØH+£©=$\frac{1{0}^{-14}}{0.01}$=10-12mol/L£¬PH=12£¬µÄPH=“×ĖįÄĘ“Ł½ųĖ®µēĄė£¬“×ĖįÄĘČÜŅŗÖŠĒāĄė×ÓÅضČĪŖ10-11mol/L£¬øł¾ŻĖ®µÄĄė×Ó»ż³£ŹżÖŖ£¬ĒāŃõøłĄė×ÓÅØ¶ČµČÓŚ10-3 mol/L£¬
¹Ź“š°øĪŖ£ŗ2£»12£»10-3 mol/L£»
£Ø3£©“×ĖįŹĒČõµē½āÖŹ£¬ĀČ»ÆĒāŹĒĒæµē½āÖŹ£¬Ļ”ŹĶ»į“Ł½ų“×ĖįµÄµēĄė£¬Čō½«“×ĖįŗĶŃĪĖįĻ”ŹĶĻąĶ¬µÄ±¶Źż£¬“×ĖįµÄpH»į±ČŃĪĖįŠ”£¬Ņņ“ĖČōŅŖŹ¹“×ĖįŗĶŃĪĖįĻ”ŹĶŗóČÜŅŗµÄpHČŌČ»ĻąµČ£¬Ōņ“×ĖįŅŖĻ”ŹĶµÄ±¶ŹżŅŖøü“óŅ»µć²ÅÄÜĀś×ćŅŖĒó£¬mŠ”ÓŚn£¬
¹Ź“š°øĪŖ£ŗŠ”ÓŚ£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµÄµēĄė”¢Ėį¼ī»ģŗĻČÜŅŗ¶ØŠŌÅŠ¶ĻµČÖŖŹ¶µć£¬øł¾ŻČõµē½āÖŹµēĄėĢŲµć¼°Ėį¼īÖŠŗĶ·“Ó¦Ą“·ÖĪö½ā“š£¬Ć÷Č·ĪļÖŹµÄŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ŌŁ½įŗĻ»ł±¾øÅÄī”¢pHµÄ¼ĘĖć”¢ĪļĮĻŹŲŗćµČÖŖŹ¶µć·ÖĪö£¬ĢāÄæÄѶČÖŠµČ£®


 Ė«»łĶ¬²½µ¼ŗ½ŃµĮ·ĻµĮŠ“š°ø
Ė«»łĶ¬²½µ¼ŗ½ŃµĮ·ĻµĮŠ“š°ø »ĘøŌŠ”דŌŖĶ¬²½¼ĘĖćĢģĢģĮ·ĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖĶ¬²½¼ĘĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃéA | ŹµŃéB | |
| ²Ł×÷ | ŌŚ×¢ÉäĘ÷ÖŠ¼ÓČė¹żĮæĆ¾Ę¬£Ø²ĮČ„±ķĆęŃõ»ÆĤ£©£¬ĪüČė15mL±„ŗĶNaHCO3ČÜŅŗ£® | ŌŚ×¢ÉäĘ÷ÖŠ¼ÓČė¹żĮæĆ¾Ę¬£Ø²ĮČ„±ķĆęŃõ»ÆĤ£©£¬ĪüČė15mLÕōĮóĖ®£® |
| ĻÖĻó | ÓŠĘųĢå²śÉś£¬20minŗó×¢ÉäĘ÷ÄŚ±ŚŗĶµ×²æ²śÉś“óĮæ°×É«³Įµķ | »ŗĀż²śÉśĘųĢå |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ūŗĻ·Ö×ÓĶØŹ½CnH2n+2µÄĢžŅ»¶Ø¶¼ŹĒĶéĢž£¬·Ö×ÓÖŠ¾łÖ»ŗ¬µ„¼ü | |
| B£® | ĶعżŹÆÓĶĮŃ»ÆæÉŅŌµĆµ½¶ąÖÖĘųĢ¬¶ĢĮ“Ģž£¬ĘäÖŠ°üĄØÖŲŅŖ»Æ¹¤ŌĮĻ | |
| C£® | ±½ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĖµĆ÷±½»·½į¹¹ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü | |
| D£® | ŅŅ“¼æÉŅŌ±»ŃõĘųŃõ»Æ³ÉŅŅĖį£¬µ«ŅŅĖįĪŽ·ØŌŁ±»ŃõĘųŃõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé | ĻÖĻó | ½įĀŪ |
| A | ĻņFeBr2ČÜŅŗÖŠ¼ÓČėÉŁĮæĀČĖ®£¬ŌŁ¼Ó CCl4Õńµ“ | CCl4²ćĪŽÉ« | Fe2+µÄ»¹ŌŠŌĒæÓŚBr- |
| B | ĻņŃĪĖįÖŠµĪČėÉŁĮæNaAlO2ČÜŅŗ | ĪŽĆ÷ĻŌĻÖĻó | AlO2-ÓėH+Ī“·¢Éś·“Ó¦ |
| C | ĻņijČÜŅŗĄļµĪ¼ÓNaOHČÜŅŗ²¢½«ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½ĮDÓŚŹŌ¹ÜæŚ | ŹŌÖ½ŃÕÉ«ĪŽ Ć÷ĻŌ±ä»Æ | ŌČÜŅŗÖŠĪŽNH4+ |
| D | ³£ĪĀĻĀ£¬²ā¶ØµČĪļÖŹµÄĮæÅØ¶ČµÄ Na2CO3ŗĶNa2SO3ČÜŅŗµÄpH | Ē°ÕßµÄpH ±ČŗóÕߵēó | ŌŖĖŲ·Ē½šŹōŠŌ£ŗS£¾C |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ·“Ó¦Īļ | ²śĪļ |
| ¢Ł | KMnO4”¢H2O2”¢H2SO4 | K2SO4”¢MnSO4 |
| ¢Ś | Cl2”¢FeBr2 | FeCl3”¢FeBr3 |
| ¢Ū | MnO4-”¢Cl- | Cl2”¢Mn2+ |
| A£® | µŚ¢Ł×é·“Ó¦µÄĘäÓą²śĪļĪŖH2OŗĶO2 | |
| B£® | µŚ¢Ś×é·“Ó¦ÖŠ²Ī¼Ó·“Ó¦µÄCl2ÓėFeBr2µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2 | |
| C£® | µŚ¢Ū×é·“Ó¦ÖŠÉś³É1molCl2£¬×ŖŅʵē×Ó2mol | |
| D£® | Ńõ»ÆŠŌÓÉĒæµ½ČõĖ³ŠņĪŖMnO4-£¾Cl2£¾Fe3+£¾Br2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
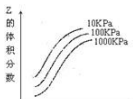
| A£® | ÉĻŹöæÉÄę·“Ó¦µÄÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦ | |
| B£® | X”¢Y”¢Z ¾łĪŖĘųĢ¬ | |
| C£® | X ŗĶ Y ÖŠÖ»ÓŠŅ»ÖÖŹĒĘųĢ¬£¬Z ĪŖĘųĢ¬ | |
| D£® | ÉĻŹö·“Ó¦µÄÕż·“Ó¦µÄ”÷S£¼0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«2mL 0.5mol•L-1Na2SiO3ČÜŅŗµĪČėĻ”ŃĪĖįÖŠÖʵĆH2SiO3½ŗĢ壬Ėłŗ¬½ŗĮ£ŹżĪŖ0.001NA | |
| B£® | ĒāŃõČ¼ĮĻµē³ŲÕż¼«ĻūŗÄ22.4L£Ø±ź×¼×“æö£©ĘųĢåŹ±£¬µēĀ·ÖŠĶعżµÄµē×ÓŹżÄæĪŖ2NA | |
| C£® | ±ź×¼×“æöĻĀ£¬20g D2O·Ö×ÓÖŠĖłŗ¬ÖŠ×ÓŹżĪŖ10NA | |
| D£® | ½«1mol Cl2ĶØČėĖ®ÖŠ£¬HClO”¢Cl-”¢ClO-Į£×ÓŹżÖ®ŗĶĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
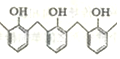 ”µÄøß¾ŪĪļ£¬Ę䵄ĢåŹĒ¼×Č©ŗĶ±½·Ó
”µÄøß¾ŪĪļ£¬Ę䵄ĢåŹĒ¼×Č©ŗĶ±½·Ó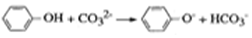
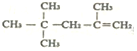 µÄĆū³ĘĪŖ£ŗ2£¬4£¬4£¬-Čż¼×»ł-1-ĪģĻ©
µÄĆū³ĘĪŖ£ŗ2£¬4£¬4£¬-Čż¼×»ł-1-ĪģĻ©| A£® | 4 | B£® | 5 | C£® | 6 | D£® | 7 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com