
【题目】阅读下列材料,完成相应填空
某同学设计了如下装置用于制取SO2和验证SO2的性质。已知:1.0mol/L的Fe(NO3)3溶液的![]() 。试回答以下问题:
。试回答以下问题:
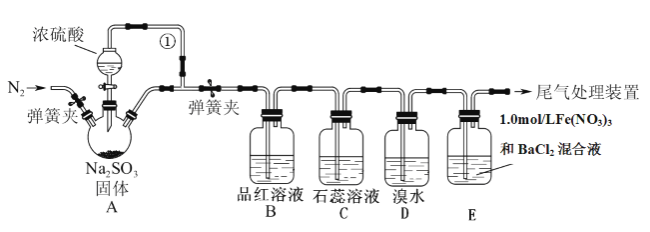
(1)装置A中用于添加浓硫酸的仪器名称为________________________,导管①的作用是______________________。
(2)B、C、D三个装置分别先后验证了SO2的哪些性质_______。
A.吸附性、酸性、还原性 B.还原性、酸性、还原性
C.漂白性、酸性、还原性 D.漂白性、酸性、氧化性
(3)SO2和品红反应的原理是_______________________________。
(4)实验前鼓入N2的目的是____________________________,简述此操作是否有必要_______________________________
(5)装置E中产生了白色沉淀,其成分是______________(填名称),分析E中产生白色沉淀的可能原因及观察到的现象。(写两种)可能①:_____________________;现象:___________。可能②:_____________________;现象:___________。
(6)若用2.0mol/L 的NaOH溶液吸收SO2尾气,请画出该尾气吸收装置_______。
【答案】分液漏斗 平衡压强,使分液漏斗内液体能够顺利流下 C 与品红作用生成不稳定的无色物质 排净装置中的空气 有必要,防止溶液中SO2被空气中的O2氧化而干扰E中实验 BaSO4 SO2与Fe3+反应生成SO42- 溶液由棕黄色变为浅绿色 在酸性条件下SO2与NO3-反应生成SO42- 溶液中有气泡产生 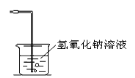
【解析】
反应产生气体,气压变大,若没有导管①平衡压强,分液漏斗内液体不能够顺利流下;因二氧化硫具有漂白性,则B中的品红溶液褪色,二氧化硫与水反应生成亚硫酸,遇石蕊变红,说明二氧化硫为酸性气体;D中二氧化硫与碘水发生氧化还原反应生成硫酸和HBr酸,该反应为SO2+Br2+2H2O═2HBr+H2SO4,二氧化硫中S元素的化合价升高,说明二氧化硫具有还原性;SO2和品红反应的原理是与品红作用生成不稳定的无色物质;氧气能将二氧化硫氧化,所以鼓入氮气的目的是排净空气防止干扰实验;二氧化硫具有还原性,酸性条件下,能被硝酸根离子或铁离子氧化生成硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;①若二氧化硫和铁离子发生氧化还原反应生成硫酸根离子和亚铁离子,硫酸根离子和钡离子反应生成白色沉淀,溶液由黄色变为浅绿色,所以除产生沉淀外,还应观察到的现象是静置一段时间后,溶液由棕黄色变为浅绿色;②若酸性条件下,硝酸根离子和二氧化硫发生氧化还原反应生成硫酸根离子和NO气体,硫酸根离子和钡离子反应生成硫酸钡白色沉淀。
(1)该仪器名称为分液漏斗;反应产生气体,气压变大,若没有导管①平衡压强,分液漏斗内液体不能够顺利流下;
(2)B中的品红溶液褪色,因二氧化硫具有漂白性;二氧化硫与水反应生成亚硫酸,遇石蕊变红,则实验现象为变红,说明二氧化硫为酸性气体;D中二氧化硫与碘水发生氧化还原反应生成硫酸和HBr酸,该反应为SO2+Br2+2H2O═2HBr+H2SO4,二氧化硫中S元素的化合价升高,说明二氧化硫具有还原性;
(3)SO2和品红反应的原理是与品红作用生成不稳定的无色物质;
(4)氧气、硝酸根离子都能将二氧化硫氧化,所以如果装置中含有氧气,会干扰实验,所以排入氮气的目的是排净空气防止干扰实验;
(5)二氧化硫具有还原性,酸性条件下,能被硝酸根离子或铁离子氧化生成硫酸根离子,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;①若二氧化硫和铁离子发生氧化还原反应生成硫酸根离子和亚铁离子,硫酸根离子和钡离子反应生成白色沉淀,溶液由黄色变为浅绿色,所以除产生沉淀外,还应观察到的现象是静置一段时间后,溶液由棕黄色变为浅绿色;②若酸性条件下,硝酸根离子和二氧化硫发生氧化还原反应生成硫酸根离子和NO气体,硫酸根离子和钡离子反应生成硫酸钡白色沉淀;
故答案为:SO2与Fe3+反应生成SO42-;静置一段时间后,溶液由棕黄色变为浅绿色;在酸性条件下SO2与硝酸根反应生成SO42-;溶液中有气泡产生;
(6)使用氢氧化钠溶液吸收多余的二氧化硫,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
(ⅰ)2H2(g)+CO(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
(ⅱ)2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2
CH3OCH3(g)+H2O(g) ΔH2
(1)则4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g)的ΔH=___(用含ΔH1、ΔH2的式子表示)
CH3OCH3(g)+H2O(g)的ΔH=___(用含ΔH1、ΔH2的式子表示)
(2)在恒容密闭容器中发生反应(ⅰ),
(Ⅰ)如图能正确反映平衡体系中甲醇体积分数随温度变化情况的曲线是__(填“a”或“b”);
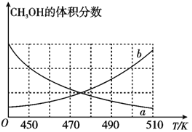
(Ⅱ)下列说法能表明反应(ⅰ)已达平衡状态的是__;
a.容器中气体的压强不再变化 b.混合气体的密度不再变化
c.混合气体的平均相对分子质量不再变化 d.v正(H2)=2v正(CH3OH)
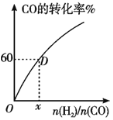
(Ⅲ)300℃下,CO的转化率与起始投料比![]() 的变化关系如图所示,测得D点氢气的转化率为40%,x=__。
的变化关系如图所示,测得D点氢气的转化率为40%,x=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2 (g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到平衡后,若扩大容器体积,则平衡逆向移动
B.若单位时间内生成x mol NO,同时消耗x mol NH3,则达到平衡状态
C.达到化学平衡时,4υ正(O2)= 5υ逆(NO )
D.化学反应速率关系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)![]() Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
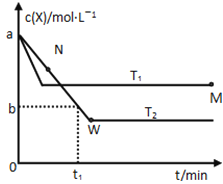
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,υ(Y)=![]() mol/(L·min)
mol/(L·min)
C.M点的正反应速率υ正大于N点的逆反应速率υ逆
D.M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Na2S2,其溶液显黄色并有强碱性。
(1)写出该反应的化学方程式:___________________________________。并写出Na2S2的电子式___________该物质中所具有的化学键的类型_______________;该反应中的Na2S表现了_____________性,当生成1mol Na2S2时,转移电子数目为___________。
(2)在碱性溶液中,多硫化钠Na2Sx(x≥2),可被NaClO氧化为硫酸钠,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则X的值为________。
A.5 B.4 C.3 D.2
(3)常温下Na2S溶液显______(填酸性、中性或碱性),理由是(用离子方程式表示)__________________________。
(4)常温pH=10的0.1mol/LNaHS溶液中各离子浓度由大到小的顺序是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应的化学方程式中,属于水解反应的是( )
A.H2O+ H2O![]() H3O++OH-
H3O++OH-
B.CO2+H2O![]() H2CO3
H2CO3
C.HCO3-+OH-![]() H2O+CO32-
H2O+CO32-
D.CO32-+ H2O![]() HCO3- +OH-
HCO3- +OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)。

①实验1、2研究的是__________对H2O2分解速率的影响。
②实验2、3的目的是_______________对H2O2分解速率的影响。
(2)查文献可知,Cu2+对H2O2分解也有催化作用,为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

①定性如图甲可通过观察_______,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是_________。
②定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是__________。
(3)酸性高锰酸钾溶液和草酸溶液可发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,实验时发现开始反应速率较慢,溶液褪色不明显,但一段时间后突然褪色,反应速率明显加快。对此展开讨论:
①某同学认为KMnO4与H2C2O4的反应是______热反应,导致_______________;
②从影响化学反应速率的因素看,你认为还可能是________的影响。要证明你的猜想,实验方案是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com