
����Ŀ��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ���������µ�ʵ��װ�á�
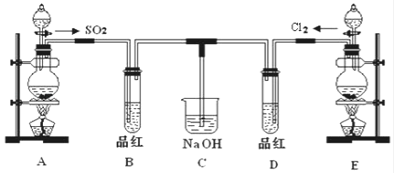
��1��ʵ������װ��A�Ʊ�SO2 ��ijͬѧ��ʵ��ʱ���ִ�A�ķ�Һ©��������©����Һ��δ���£�����Ϊԭ�������______��
��2��ʵ������װ��E�Ʊ�Cl2 ���䷴Ӧ�����ӷ���ʽΪ_____������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ�������Ϊ_____��
��3��ֹͣͨ�����ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�ΪB��_______��D��_______��
��4����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ���������������������������������ԭ���û�ѧ����ʽ��ʾ��__________��
���𰸡���1����Һ©���IJ�����û��ȡ����
��2��MnO2+4H++2Cl��![]() Mn2++Cl2��+2H2O��1.806��1024
Mn2++Cl2��+2H2O��1.806��1024
��3����ɫ��Ʒ���ָֻ��ɺ�ɫ ������������
��4��Cl2+SO2+2H2O=2HCl+H2SO4
��������
���⣨1������û��ȡ����������ʱ�������������Һ©���ڲ�����ɷ�Һ©���ڵ�ѹǿС�ڴ���ѹǿ��Һ��������������©����Һ��δ���µ�ԭ���Ƿ�Һ©���IJ�����û��ȡ������
��2��װ��E��ʵ������������װ�ã�MnO2��Ũ���ᷴӦ�����Ȼ��̡�������ˮ����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl��![]() Mn2++Cl2��+2H2O���������ӷ���ʽ��ÿ��4mol HCl���뷴Ӧ��ת��2mol���ӣ�����6 mol��HCl�μӷ�Ӧʱ��ת�Ƶĵ�������Ϊ3NA=3��6.02��1023=1.806��1024��
Mn2++Cl2��+2H2O���������ӷ���ʽ��ÿ��4mol HCl���뷴Ӧ��ת��2mol���ӣ�����6 mol��HCl�μӷ�Ӧʱ��ת�Ƶĵ�������Ϊ3NA=3��6.02��1023=1.806��1024��
��3��SO2����Ư���ԣ���������ͨ��Ʒ����Һ�У�Ʒ����ɫ��SO2��Ư���п����ԣ���ɫ�����Һ����ʱ�ָֻ�ԭ���ĺ�ɫ��������ˮ��Ӧ���ɵĴ��������Ư���ԣ��������ͨ��Ʒ����Һ��Ҳ��ʹƷ����ɫ���������Ư�ײ����棬����ʱ�����ָܻ���ɫ�����������Թ��е�����ֱ�Ϊ��ɫ��Ʒ���ָֻ��ɺ�ɫ������������
��4���������н�ǿ�������ԣ�����������н�ǿ�Ļ�ԭ�ԣ���ˮ��Һ������1��1������Ӧ��Cl2+SO2+2H2O=2HCl+H2SO4�������ﶼ��Ư���ԣ����SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һʱ��Ʒ����Һ������ɫ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭп�Ͻ��ƳɵĻ�ͭ��Ʒò�ƻƽ����з���������������α����
A.��۹۲�B.����������C.�ⶨ�ܶ�D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����仯����������������Ӧ�ù㷺���ش��������⣺
��1����立���һ�ֻ�ѧ���ʣ�����ʽ��NH4Fe(SO4)2��12H2O��������ˮ����Һ�е�����Ũ�ȴ�С��ϵΪ_____________________��
��2����֪ij��Һ�к���CO32����SO42�������ӣ�ȡһ�����ĸ���Һ�������еμ�BaCl2��Һ����CO32����ʼ����ʱ����Һ��![]() ��_____������֪Ksp(BaSO4)=1.0��10��10��Ksp(BaCO3)=2.5��10��9��
��_____������֪Ksp(BaSO4)=1.0��10��10��Ksp(BaCO3)=2.5��10��9��
��3����֪��S2Cl2(l)��Cl2(g)��2SCl2(l)����H����50.2 kJ��mol��1������1mol Cl��Cl����1mol S��S���ֱ���Ҫ����243kJ��268kJ�������������1mol S��Cl����Ҫ���յ�����Ϊ_____________kJ��
��4��ij�ݻ�������ܱ������з������·�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g) ��H=��197 kJ��mol��1��
2SO3(g) ��H=��197 kJ��mol��1��
��������˵����Ӧ�ﵽƽ��״̬���� ________________
a����ϵѹǿ���ֲ��� b�����������ܶȱ��ֲ���
c��SO3��O2������ȱ��ֲ��� d��ÿ����1 mol SO3��ͬʱ����1 mol SO2
����ͬ�¡�ͬ����������ܱ������зֱ�������壺(��)2 mol SO2 ��1 mol O2��(��) 1 mol SO2 ��0.5 mol O2 �����¡������·�Ӧ��ƽ��ʱ�����������ڵ�ѹǿ��С��ϵΪ____����p����p����ʾ����
��5����NaOH��Һ���������е�SO2�������õ�Na2SO3��Һ���е�⣬�����Ʊ�H2SO4����ԭ������ͼ��ʾ(�缫����Ϊʯī)��
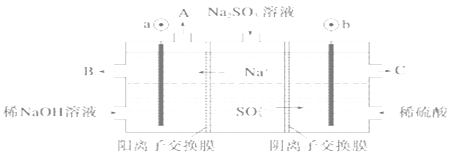
�����ĵ缫��ӦʽΪ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ�˼���Ũ������ľ̿���ڼ��������·�Ӧ����������������ѡ��������ͼ��ʾ��ʵ��װ�á�
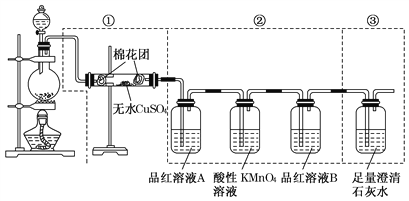
(1)д��Ũ������ľ̿���ڼ��������µĻ�ѧ����ʽ______________________��
(2)������ˮ����ͭ��������___________________________��
(3)��������KMnO4��Һ��������__________________________��
(4)���������õ�Ʒ����Һ�����ǵ����÷ֱ���
A_____________________�� B ___________________ ��
(5)���г��ֵ�����____________________________________________________��
������Ӧ�����ӷ���ʽ_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ������ɫʯ����ֽ���ڲ���Ƭ�ϣ�Ȼ��˳��ֱ�μ�65%��HNO3��98%��H2SO4�����Ƶ���ˮ��������ֽ���ֵ���ɫ�ֱ���(����)
A.�ס��ڡ���B.�졢�ڡ���C.�졢�졢��D.�ס��ڡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SrSO4���������̻���մɹ�ҵ������Na2SO4��Һ�м���������Һ�������á���ͼ��ʾ��ͬ�¶��£�SrSO4��Һ��lg[c( Sr2+)]��lg[c( SO42��)]֮��Ĺ�ϵ�������й�˵����ȷ���� �� ��
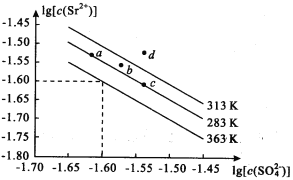
A. ͼ����a ��c������ܶȻ�Ksp ( a ) < Ksp ( c )
B. 363KʱKsp (SrSO4) = 1.0��10��3.2
C. SrSO4���ܽ�����¶����߶�����
D. 313Kʱ��b���Ӧ����ҺΪ������Һ��d���Ӧ����ҺΪ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ձ���������ĺ�й©�з�����������Ҫ��Cs��131I�������й�127I��131I��˵����ȷ���ǣ� ��
A. 127I��131I��Ϊͬλ�� B. 127I��131I��Ϊͬ��������
C. 127I��131I��ͬ���칹�� D. I��Cl������A�壬I��Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��H2(g)��F2(g)===2HF(g)����H����546.6 kJ/mol������˵����ȷ���� (�� ��)
A. ����������ֽ����������ͷ����ķ�Ӧ�Ƿ��ȷ�Ӧ
B. 1 mol H2��1 mol F2��Ӧ����2 molҺ̬HF�ų�������С��546.6 kJ
C. ����ͬ�����£�1 mol H2��1 mol F2�������ܺʹ���2 mol HF������
D. �÷�Ӧ�е������仯������ͼ����ʾ

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ҵ���˵���������
A.����ȼ��B.�ܶȱ�ˮ��
C.��ˮ����Ȼ���D.�ܷ���������Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com