
| A. | 碳酸钠粉末 | B. | 冰醋酸 | C. | 硝酸钾溶液 | D. | 硫酸钠溶液 |
分析 反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,注意Zn过量,以此来解答.
解答 解:A.加入碳酸钠,与酸反应,生成氢气的量减少,故A错误;
B.加入冰醋酸,导致氢离子物质的量增多,所以生成氢气的量增大,故B错误;
C.加入硝酸钾,相当于含有硝酸,硝酸和锌反应生成氮氧化物而不是氢气,故C错误;
D.加入硫酸钠溶液导致溶液中氢离子浓度降低,反应速率减小,但氢离子总物质的量不变,所以生成氢气总量不变,故D正确;
故选D.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度对反应速率的影响即可解答,易错选项是C,注意硝酸和金属反应生成氮氧化物而不是氢气,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,22 gCO2 中含有NA个氧原子 | |
| B. | 1mol/L CaCl2溶液中Cl-的数目等于2NA | |
| C. | 标准状况下,33.6LCH4中含H原子数为6NA | |
| D. | 1ol Na 完全反应时,失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,1L一氧化碳气体一定比1L氧气的质量小 | |
| B. | 任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 | |
| C. | 同温同压下的二氧化碳气体和氮气,若体积相等,则质量一定相等 | |
| D. | 同温同压下,相同体积的气体,其分子数一定相等,原子数也一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量晶体放入试管中,加热,若试管口上蘸有少量无水硫酸铜粉末的脱脂棉变蓝,则可证明晶体中含有结晶水 | |
| B. | 取少量晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量晶体放入试管,加入少量稀NaOH溶液,在试管口用湿润的蓝色石蕊试纸检验,若变红,则可证明晶体的成分中含有NH4+ | |
| D. | 取少量晶体溶于水,加适量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
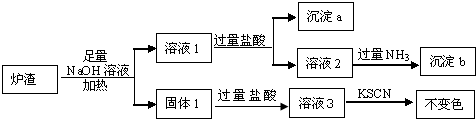
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com