
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】关于化学对社会进步和人类文明的贡献,下列说法不正确的是( )
A.化石燃料的直接利用,促进了低碳经济的发展
B.新材料的研制和应用,提高了人们的生活品质
C.合成药物的研发和使用,促进了医疗卫生事业的发展
D.化肥的合理使用提高了农作物产量,缓解了人类粮食危机
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3.9gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2的体积(标准状况);
(2)反应后所得NaOH的物质的量浓度(反应前后溶液体积变化忽略不计).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的说法正确的是( )
A.当△H为“﹣”时,表示该反应为吸热反应
B.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.已知:C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5 kJ/mol,碳的燃烧热为110.5 kJ/mol
O2(g)═CO(g)△H=﹣110.5 kJ/mol,碳的燃烧热为110.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
A.铜器出现铜绿[Cu2(OH)2CO3]B.铁制菜刀生锈
C.大理石雕像被酸性较强的雨腐蚀毁坏D.铝锅表面生成致密的薄膜(Al2O3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同条件下,下列各组热化学方程式中,△H2>△H1的是( )
A.2H2 (g)+O2(g)═2H2O(g)△H1; 2H2(g)+O2(g)═2H2O(l)△H2
B.S(g)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(g)△H2
C.CO(g)+ ![]() ?O2(g)═CO2(g)△H1; 2CO(g)+O2(g)═2CO2(g)△H2
?O2(g)═CO2(g)△H1; 2CO(g)+O2(g)═2CO2(g)△H2
D.![]() ?H2(g)+
?H2(g)+ ![]() ?Cl2(g)═HCl(g)△H1;H2(g)+Cl2(g)═2HCl(g)△H2
?Cl2(g)═HCl(g)△H1;H2(g)+Cl2(g)═2HCl(g)△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,有白色沉淀产生且不再变化的是( )
A. 把CO2通入澄清石灰水中至过量
B. 向AlCl3溶液中不断滴入氨水至过量
C. 把NaOH溶液逐滴滴加到Al2(SO4)3溶液中至过量
D. 把CO2通入CaCl2溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按下图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
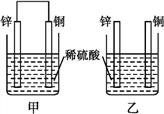
(1)下列说法中正确的是____(填序号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减小、乙中锌片质量减小 D.两烧杯中H+的浓度均减小
(2)当甲中产生1.12 L(标准状况)气体时,理论上通过导线的电子数目为____。
(3)当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L1。试确定原稀硫酸中c(H2SO4)=___________。
(4)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为 KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池总反应的化学方程式:________________________。
(5)以甲醇(CH3OH)为燃料的电池中,电解质溶液为酸性,负极的反应式为:_______________________,正极的反应式为:___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com