
��֪Ksp(AgCl)��1.6��10��13��Ksp(AgI)��1.0��10��16�����й��ڲ�����֮��ת����˵���д������
����A��AgCl������ˮ������ת��ΪAgI
����B�����ֲ������Ksp���Խ�������Խ����ת��Ϊ�����ܵIJ�����
����C��AgI��AgCl��������ˮ������AgCl����ת��ΪAgI
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻����
2.5��10��10mol/L
 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܻ�����ı�����Һ�����ܽ�ƽ��,����:AgCl(s)![]() Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) ![]() 2Ag++
2Ag++![]() ����һ���¶���,��֪:Ksp(AgCl)=c(Ag+)��c(Cl-)=1.8��10-10,Ksp(Ag2CrO4)=��c(Ag+)��2��c(
����һ���¶���,��֪:Ksp(AgCl)=c(Ag+)��c(Cl-)=1.8��10-10,Ksp(Ag2CrO4)=��c(Ag+)��2��c(![]() )=1.9��10-12,����0.01 mol��L-1 AgNO3��Һ�ζ�0.01 mol��L-1 KCl��0.001 mol��L-1 K2CrO4�����Һ,ͨ������ش�:
)=1.9��10-12,����0.01 mol��L-1 AgNO3��Һ�ζ�0.01 mol��L-1 KCl��0.001 mol��L-1 K2CrO4�����Һ,ͨ������ش�:
(1)Cl-��![]() ˭�ȳ���?
˭�ȳ���?
(2)���ճ���Ag2CrO4����ʱ,��Һ��Cl-�����ʵ���Ũ���Ƕ���?(������Һ�ڷ�Ӧ���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�콭��ʡ��ͨ��ͨ��������4�²�©��ȱר���⻯ѧ�Ծ����������� ���ͣ�������
(12��)�Ȼ�������SO2Cl2����Ҫ�����Ȼ���������һ����ɫҺ�壬�۵㡪54.1�棬�е�69.1�棬��ˮ����������Ȼ��⡣�Ȼ��������ø���Ķ�������������ڻ���̿���������·�Ӧ��ȡ��SO2(g)��Cl2(g) SO2Cl2(l) ��H����97.3kJ/mol
SO2Cl2(l) ��H����97.3kJ/mol
��Ϊ�����������Ӧ��Cl2��ƽ��ת���ʣ����д�ʩ�������� ���ñ����գ���
| A����С������� | B��ʹ�ô��� | C������SO2Ũ�� | D�������¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���Ĵ�ʡ����������ٸġ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
ij��糧������β��ͨ�뱥��K2CO3��Һ���ճغ��ֽ���Ƶô�����CO2�����ںϳ�����H2��Ӧ���ɼ״����乤��������ʾ��ͼ����:

��1�����ճ��б���K2CO3��Һ����CO2�����ӷ���ʽ�� ��
��2������ʾ��ͼ��ѭ��ʹ�õ������� ��
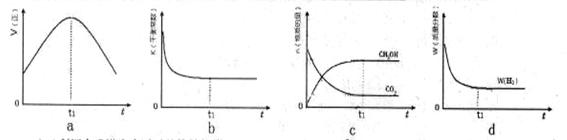
��3��300��ʱ���ϳ����еķ�ӦΪCO2(g)��3H2(g)  CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)
CH3OH(g)��H2O(g)�����ܱ������£�����ʾ��ͼ��˵����Ӧ���е�t1ʱ��ʱ�ﵽƽ��״̬���� (����ĸ���)
��4�����úϳ�����ʧ���ĸ�п��ý���Ƶú���Cl- ��CrO42- ����Һ����Ũ�Ⱦ�Ϊ0.01mol/L�������Һ����μ���0.01mol/L��AgNO3��Һʱ�����Ȳ����������������� (��֪:Ksp(AgCl)=1.56��10-10��Ksp(Ag2CrO4)=9.0��10-12)
��5���ϳ�����ʧ��ĸ�п��ý�������Ʊ�п�̵�ء��ڼ��������£��õ�ص��ܷ�ӦΪ��Zn(s) ��2MnO2(s) ��H2O(l) = Zn(OH)2(s) ��Mn2O3(s) ���õ�������ĵ缫��Ӧʽ�� �����õ�ص��(���Ե缫)������Mg(NO3)2��NaCl�Ļ����Һ���������������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��ɽ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪Ksp(AgCl)=1.8��10��10mol2•L��2��Ksp(AgI)=1.0��10��16mo2•L��2������˵���������
A��AgCl������ˮ������ת��ΪAgI
B���ں�Ũ�Ⱦ�Ϊ0.001mol•L��1��Cl����I������Һ�л�����AgNO3ϡ��Һ��������AgI
C��AgI��AgCl��������ˮ������AgCl��ת��ΪAgI
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻���� ��10��11mol•L��1
��10��11mol•L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���Ĵ�ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪Ksp(AgCl )=1.8��10��10��Ksp(AgI)��1.0��10��16�����й��ڲ�����֮��ת����˵���д�����ǣ� ��
A��AgCl������ˮ������ת��ΪAgI
B�����ֲ������Ksp���Խ�������Խ����ת��Ϊ�����ܵIJ�����
C��AgI��AgCl��������ˮ�����ԣ�AgCl����ת��ΪAgI
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻���� ��10��11
mol��L��1
��10��11
mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com