
| A. | 过量铁加入到稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO2↑+4H2O | |
| B. | 向AgCl悬浊液中滴加饱和KI溶液 AgCl+I-═AgI+Cl- | |
| C. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+H2O═2Al(OH)3↓+HCO3- | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
分析 A.铁与稀硝酸反应生成硝酸亚铁和NO气体;
B.碘化银的溶解度小于氯化银,实现了沉淀的转化;
C.离子方程式两边负电荷不相等,违反了电荷守恒;
D.澄清石灰水过量,反应后不会剩余碳酸根离子.
解答 解:A.过量铁加入到稀硝酸中,反应生成硝酸亚铁和NO,正确的离子方程式为:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,故A错误;
B.向AgCl悬浊液中滴加饱和KI溶液,氯化银沉淀转化成碘化银,反应的离子方程式为:AgCl+I-═AgI+Cl-,故B正确;
C.向NaAlO2溶液中通入过量CO2,反应生成氢氧化铝沉淀和碳酸氢钠,正确的离子方程式为:2AlO2-+2CO2+4H2O═2Al(OH)3↓+2HCO3-,故C错误;
D.NaHCO3溶液中加入过量的澄清石灰水,反应生成碳酸钙沉淀、水和氢氧化钠,反应的离子方程式为:2HCO3-+2Ca2++2OH-═2CaCO3↓+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).


科目:高中化学 来源: 题型:选择题
| A. | 气体分子间的平均距离 | B. | 气体的分子的形状 | ||
| C. | 气体分子本身的大小 | D. | 气体分子的种类 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
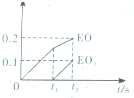 将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.
将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯银饰品久置表面变暗属于化学腐蚀 | |
| B. | 温度越高,金属发生化学腐蚀的速率越快 | |
| C. | 金属腐蚀就是金属失去电子被氧化的过程 | |
| D. | 铁门上的铜铆钉处在潮湿的空气中直接发生反应:Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E元素的+3价离子有5个未成对电子 |
| F在周期表的第15列 |
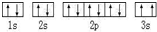 B电子排布图如图,违背了泡利原理.
B电子排布图如图,违背了泡利原理.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氨水中通入HCl气体,溶液导电性增强 | |
| B. | 向氨水中加入水,$\frac{{C}_{(O{H}^{-})}}{N{H}_{3}•{H}_{2}O}$值增大 | |
| C. | 向氨水中通入NH3,电离度增大 | |
| D. | 向氨水中加入水,Kb不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com