
A、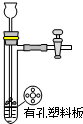 装置用于Na2SO3和浓H2SO4反应制取少量的SO2气体 |
B、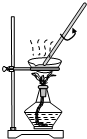 装置用于灼烧CuSO4?5H2O |
C、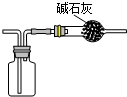 装置用于收集氯气并防止污染空气 |
D、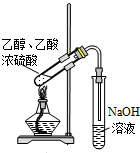 装置用于实验室制备少量乙酸乙酯 |


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
根据相关化学知识分析,下列推断正确的是
A.若X原子中的质子数为a,中子数为b,则X的质量数为:a-b
B.若弱酸HA的酸性强于弱酸HB,则同物质的量浓度钠盐溶液的碱性比较为:NaA<NaB
C.若R2-和M+的电子层结构相同,则原子序数的比较为:R>M
D.若反应A2+2D—==2A-+D2能发生,则氧化性的比较为:D2>A2
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ClO2是还原剂 |
| B、1 mol ClO2转移3mol电子 |
| C、CN-离子转化为NO2和CO2 |
| D、氧化剂与还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
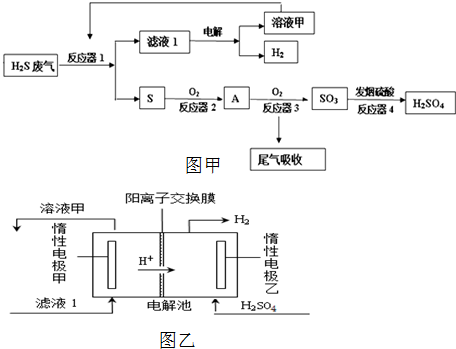
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B、淀粉、油脂和蛋白质都能发生水解反应 |
| C、多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 |
| D、汽油、柴油和植物油都是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 实验现象 | 结论 | |
| A | 向某溶液中加入氯化钡、稀硝酸的混合液 | 产生白色沉淀 | 该溶液中一定含有SO42-或SO32- |
| B | 将某气体通入品红溶液 | 溶液红色褪去 | 该气体一定SO2 |
| C | 把湿润的碘化钾--淀粉试纸放入某一红棕色的气体中 | 试纸变蓝色 | 该气体可能是NO2 |
| D | 将通入SO2到酸性高锰酸钾溶液中 | 溶液紫色褪去 | SO2具有漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 二甲醚(CH3OCH3)可作为洁净的液体化石燃料,以CO和H2为原料生产二甲醚的一种工艺主要发生以下三个反应:
二甲醚(CH3OCH3)可作为洁净的液体化石燃料,以CO和H2为原料生产二甲醚的一种工艺主要发生以下三个反应:| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1=-91kJ?mol-1 | K1 |
| ② | 2CH3OH(g)?CH2OCH3(g)+H2O(g)△H1=-24kJ?mol-1 | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H1=-4kJ?mol-1 | K3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com