



科目:高中化学 来源: 题型:
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、浓硫酸在常温下可迅速与铜片反应而放出二氧化硫 |
| C、浓硫酸是一种干燥剂,能用来干燥氨气、氢气 |
| D、浓硫酸在常温下能够使铁铝钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、试管外壁有水珠不一定要擦干,加热时会自然挥发 | ||
| B、应握紧试管夹,大拇指按在短柄上 | ||
C、试管中液体的量不能超过试管容积的
| ||
| D、可以使试管的受热部位在火焰上方先上下移动,后集中加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物中可能含有共价键 |
| B、共价化合物中可能还有离子键 |
| C、两种元素组成的分子中一定只有极性键 |
| D、非金属元素组成的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
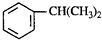 ) ⑧乙炔.按下列要求填空:
) ⑧乙炔.按下列要求填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置,实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意效果.
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置,实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意效果.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com