
 常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性.现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性.现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )| A. | 水 | B. | 澄清石灰水 | C. | 纯碱溶液 | D. | 稀盐酸 |
分析 当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性,据此分析.
解答 解:由图可以看出,当加入X物质时,遇到盐酸会反应,之后随着盐酸的消耗,加入物质能够与氯化钙反应,但是对应生成物必须是中性的,而继续加入X,溶液显碱性,所以加入物质不能是碱,但是却显碱性.
A、HCl与CaCl2的混合溶液显酸性,加入水时溶液的pH升高,但是不会等于或大于7.
B、加入石灰水时,氢氧化钙能和盐酸反应生成氯化钙和水,溶液的pH升高.当酸完全被消耗之后,继续滴加石灰水,由于和氯化钙不反应,所以pH值马上大于7,而不会出现水平等于7的一段.
C、加入纯碱溶液时,碳酸钠能和盐酸反应,也能和氯化钙反应.开始时碳酸钠和盐酸反应,导致pH上升;当酸完全被消耗时,碳酸钠和氯化钙反应,生成物都是中性的,一直到氯化钙被完全消耗;当继续滴加碳酸钠时,由于碳酸钠显碱性,所以pH大于7.
D、加入盐酸时,盐酸和氯化钙不反应,溶液的pH不能等于或大于7.
故选C.
点评 本题主要考查了溶液的酸碱性和溶液pH的关系方面的知识,同时考查了读图能力,从图中提炼解题的关键要素.


科目:高中化学 来源: 题型:多选题
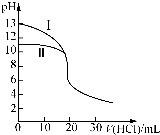 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )| A. | Ⅱ表示的是滴定氨水的曲线,当V(HCl)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-) | |
| C. | 滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 (弱碱性,易被氧化)
(弱碱性,易被氧化) 中官能团的名称氨基、羧基,②的反应类型是取代反应.
中官能团的名称氨基、羧基,②的反应类型是取代反应. 的同分异构体的结构简式
的同分异构体的结构简式 .
. +nH2O.
+nH2O. 的合成路线.
的合成路线.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )| A. | 一定条件下与氢气反应可以生成硬脂酸甘油酯 | |
| B. | 该物质不能使酸性KMnO4溶液褪色 | |
| C. | 与氢氧化钠溶液混合加热能得到肥皂的主要成分 | |
| D. | 与其互为同分异构且完全水解后产物相同的油脂还有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe和足量稀硝酸反应Fe+2H+═Fe2++H2↑ | |
| B. | 将Fe(NO3)3溶液与少量HI混合:8H++2NO3-+6I-═4H2O+3I2+2NO↑ | |
| C. | 用过量氨水吸收SO2的反应:NH3•H2O+SO2═NH4++HSO3- | |
| D. | 少量Ca(OH)2和NaHCO3反应 Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则(1)溶液中一定含有的阳离子有H+、NH4+、Mg2+、Al3+,一定不含有的离子有CO32-、NO3-、Fe3+.
100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则(1)溶液中一定含有的阳离子有H+、NH4+、Mg2+、Al3+,一定不含有的离子有CO32-、NO3-、Fe3+.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com