
A、 氨气发生装置 |
B、 氨气吸收装置 |
C、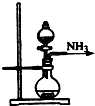 氨气发生装置 |
D、 氨气收集、检验装置 |


科目:高中化学 来源: 题型:
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B、已知,N2(g)+3 H2(g)?2NH3(g)△H<0,为提高氨的产率,理论上应采取降低温度的措施 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)△H<0,达平衡后,升高温度体系颜色变深 |
| D、对于2HI(g)?H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:2HCO3-+Ba2++2OH-=BaCO3↓+H2O+CO32- | ||||
| B、Na2S溶液吸收足量SO2:S2-+2SO2+2 H2O=2HSO3-+H2S↑ | ||||
| C、硫酸氢镁溶液中加入足量氢氧化钠:Mg2++2OHˉ=Mg(OH)2↓ | ||||
D、用铜为电极电解稀硫酸溶液:Cu+2H+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、按系统命名法:CH3CH2C(CH3)2CH(C2H5)CH3的正确名称是3,3,4-三甲基己烷 |
| B、所有的糖、油脂、蛋白质都能水解,但水解产物不同 |
C、1mol的 最多能与含5mol NaOH的水溶液完全反应 最多能与含5mol NaOH的水溶液完全反应 |
D、若完全燃烧,1mol雄酮( 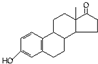 )比雌酮( )比雌酮( )多消耗3mol O2. )多消耗3mol O2. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为中学化学教材上的喷泉实验装置.在烧瓶中充满了干燥气体,胶头滴管及烧瓶中分别盛有液体,下列各组中能形成这样喷泉但液体不能充满烧瓶的是( )
如图为中学化学教材上的喷泉实验装置.在烧瓶中充满了干燥气体,胶头滴管及烧瓶中分别盛有液体,下列各组中能形成这样喷泉但液体不能充满烧瓶的是( )| A、NH3 |
| B、NO2和H2O |
| C、CO2和NaOH溶液 |
| D、4:1的NO2与O2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
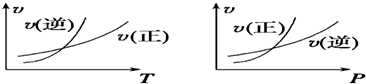
| A、b>c,正反应为放热反应 |
| B、b<c,正反应为吸热反应 |
| C、a+b>c,正反应为放热反应 |
| D、a+b<c,正反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4L的HCl含有6.02×1023个粒子 |
| B、32g氧气中含有2mol的氧原子 |
| C、氢氧化钠的摩尔质量为40g |
| D、如果有6.02×1023颗大米,则这些大米的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO是汽车尾气的有害成分之一 |
| B、NO是具有刺激性气味的红棕色气体 |
| C、NO极少量时在人体的血管系统内会促进血管扩张,防止血管栓塞 |
| D、NO能够与人体血红蛋白结合,吸入较多会造成人体缺氧中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com