
【题目】根据热化学方程式N2(g)+3H2(g)![]() 2NH3(g)+92kJ,下列有关图像和叙述中正确的是
2NH3(g)+92kJ,下列有关图像和叙述中正确的是
A.  B.
B. 
C. 向密闭容器中通入1mol氮气和3mol氢气发生反应放出92kJ的热量D. 形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量多92kJ
【答案】B
【解析】
A、依据化学反应方程式:N2(g)+3H2(g)![]() 2NH3(g)+92kJ,反应是放热反应,依据能量守恒,反应物总能量大于生成物总能量,故A错误;
2NH3(g)+92kJ,反应是放热反应,依据能量守恒,反应物总能量大于生成物总能量,故A错误;
B、已知:N2(g)+3H2(g)![]() 2NH3(g)+92kJ,反应是放热反应,依据能量守恒,反应物总能量大于生成物总能量,1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3(g)的能量,故B正确;
2NH3(g)+92kJ,反应是放热反应,依据能量守恒,反应物总能量大于生成物总能量,1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3(g)的能量,故B正确;
C、反应是可逆反应不能进行彻底,向密闭容器中通入1mol氮气和3mol氢气发生反应,放出的热量小于92.4 kJ,故C错误;
D、已知:N2(g)+3H2(g)![]() 2NH3(g)+92kJ,正反应是放热反应,则逆反应为吸热反应,即形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量少92kJ,故D错误。
2NH3(g)+92kJ,正反应是放热反应,则逆反应为吸热反应,即形成1mol氮氮键和3mol氢氢键所放出的能量比拆开6mol氮氢键所吸收的能量少92kJ,故D错误。
故选B。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧二氧化碳⑨液态氯化氢 ⑩硫酸溶液。上述物质中能导电的是________,属于电解质的是________,属于非电解质的是____________。(填编号)
(2)3.01×1023个NH4+含有质子的物质的量是__________,含有电子的物质的量是__________;
(3)200mL 2mol/L的Al2(SO4)3溶液中SO42﹣的物质的量浓度为__________;
(4)标准状况下,36g H2和O2组成的混合气体的体积是67.2L,则混合气体中H2和O2的体积比为_____________;
(5)标准状况下,将33.6LNH3溶于水配成500mL溶液,该溶液的物质的量浓度为____________;
(6)已知1.505×1023个A气体分子的质量为31g,则A气体的摩尔质量是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体。A、B、C、D、E、F和OPA的转化关系如下所示:

回答下列问题:
(1)A的化学名称是 ;
(2)由A生成B 的反应类型是 。在该反应的副产物中,与B互为同分异构体的化合物的结构简式为 ;
(3)写出C所有可能的结构简式 ;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用化学方程式表示合成路线 ;
(5)OPA的化学名称是 ,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为 ,该反应的化学方程式为 。(提示![]() )
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2R是一种二元弱酸。25℃时,向H2R溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为![]() 或
或![]() ]与pH的变化关系如图所示。下列说法一定正确的是
]与pH的变化关系如图所示。下列说法一定正确的是

A. Ⅱ表示lg![]() 与pH的变化关系
与pH的变化关系
B. pH=1.22的溶液中:2c(R2-)+c(HR-)<c(Na+)
C. NaHR溶液中c(H+)>c(OH-)
D. 当溶液呈中性时:c(Na+)>c(HR-)>c(R2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定大量共存的是( )
A. 含有AlO2-的溶液中:Na+ 、Al3+、Cl-、K+
B. 常温下由水电离出的c(H+)·c(OH-)=10-20 mol2·L-2的溶液中:Na+、NH![]() 、Cl-
、Cl-
C. 常温下 c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
D. 在c(H+)=1.0×10-13 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,CH3COOH的电离平衡常数为K,向20mL 0.1mol/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是( )
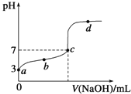
A. b点表示的溶液中c(Na+)>c(CH3COO﹣)
B. c点表示CH3COOH和NaOH恰好反应完全
C. d点表示的溶液中c(CH3COO﹣) c(H+)/c(CH3COOH)大于K
D. b、c、d三点表示的溶液中一定都存在:c(Na+)+c(H+)═c(CH3COO﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是______(填编号)。若测定结果偏高,其原因可能是________(填字母)。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.所配的标准NaOH溶液物质的量浓度偏大
(2)判断滴定终点的现象是_____________________________________。
(3)如图是某次滴定时的滴定管中的液面,其读数为________mL。

(4)根据下列数据,请计算待测盐酸的浓度:________mol·L-1。
滴定次数 | 待测体积(mL) | 标准烧碱溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中的NO与CO发生如下反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH<0,下列说法中错误的是
N2(g)+2CO2(g) ΔH<0,下列说法中错误的是
A. 该反应中反应物的总能量高于生成物的总能量
B. 升高温度,正反应速率加快,逆反应速率减慢
C. 升高温度,NO转化率减小
D. 使用合适的催化剂,能增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )

A. a点由水电离出的c(H+)=1.0×10-14 mol·L-1
B. b点:c(NH![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)=c(NH![]() )
)
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com