
| A.生成物总能量一定低于反应物总能量 |
| B.等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),放出的能量相同 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:不详 题型:问答题
 的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。| 离子 | H+ | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol·L-1 | 未测定 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
 2NO(g) △H
2NO(g) △H 0
0 0,判断该设想能否实现并简述其依据: 。
0,判断该设想能否实现并简述其依据: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ·mol-1 | a | b | c |

 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.ΔH1=ΔH-ΔH2>0 |
| B.X是反应A(g)+B(g)—→C(g)的催化剂 |
| C.E2是反应②的活化能 |
| D.ΔH=E1-E2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
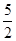 O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )| A.当转移10NA个电子时,该反应放出1300 kJ的能量 |
| B.当1NA个水分子生成且为液体时,吸收1300 kJ的能量 |
| C.当2NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
| D.当8NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2SO2+O2 2SO3 ΔH=-196.6 kJ·mol-1 2SO3 ΔH=-196.6 kJ·mol-1 |
| B.C(g)+O2(g)=CO(g) ΔH=393.5 kJ·mol-1 |
C.H2(g)+ O2(g)=H2O(g) ΔH=-241.8 kJ O2(g)=H2O(g) ΔH=-241.8 kJ |
| D.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 SO3(g) ΔH="-98.32" kJ·mol-1,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量( )
SO3(g) ΔH="-98.32" kJ·mol-1,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量( )| A.="196.64" kJ | B.="98.32" kJ |
| C.<196.64 kJ | D.>196.64 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
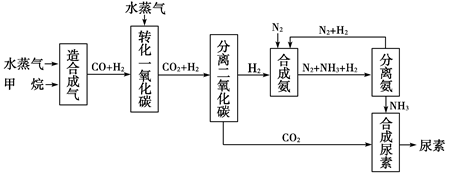
 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com