
已知:RCH2COONa![]() RCH3,今有X、Y两种有机物能发生如下转变,其关系如图:
RCH3,今有X、Y两种有机物能发生如下转变,其关系如图:
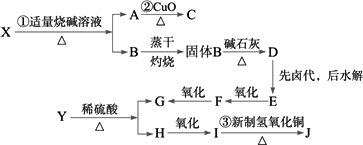
X的分子式为C5H10O2,J和X是同分异构体.只有Y、G、F、I能被新制的Cu(OH)2悬浊液氧化,H不能发生消去反应.
(1)写出X、Y的结构简式:X________;Y________.
(2)写出图中反应方程式:
①________;
②________;
③________.
答案:(1)CH3COOCH(CH3)2 ![]()
(2)①CH3COOCH(CH3)2+NaOH→CH3COONa+(CH3)2CHOH
②![]()
③C(CH3)3CHO+2Cu(OH)2![]() C(CH3)3COOH+Cu2O↓+2H2O
C(CH3)3COOH+Cu2O↓+2H2O
解析:A可以和氧化铜反应得到C,A应为醇类,所以X可以在碱性条件下水解得到A和B,X应为酯类,且X的分子式为C5H10O2,J和X是同分异构体,所以J也为C5H10O2.又因为G可以发生银镜反应,所以G为甲酸,则E中只有一个碳;根据信息可知,B中有两个碳,所以C中有三个碳,且不能发生银镜反应,所以为丙酮.所以X为CH3COOCH(CH3)2,又H不能发生消去反应,所以β碳原子无H原子,Y为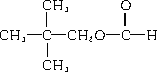 .
.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com