
����Ŀ������(N2H4)�ֳ�����������ʱ��һ�ֿ�ȼ��Һ�壬���������ȼ�ϡ�
(1)��֪��25�桢101kPaʱ��16g N2H4����������ȫȼ�����ɵ������ų�312kJ����������N2H4��ȫȼ�յ��Ȼ�ѧ����ʽ��__________________________________��
II������ͼ��ʾ��ij�о���ѧϰС����������ȼ��ԭ�����һ����(N2H4)������ȼ�ϵ��(��ͼ��)��̽��ijЩ��ҵԭ����������װ����XΪ�����ӽ���Ĥ(��ֻ����������ͨ��)��
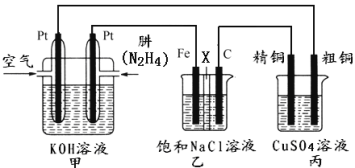
����Ҫ��ش�������⣺
(2)��װ����ͨ��________�����һ��Ϊ��������缫��ӦʽΪ��________________��
(3)��װ����ʯī�缫Ϊ_________������缫��ӦʽΪ_______________��������__________________����÷�Ӧ������һ��ʱ����ҳ��е���Һ��_______�ԡ�
(4)ͼ���ñ�װ��ģ�ҵ�е�_________________ԭ������������װ�þ�ͭ��������3.2g���������ϼ�װ��������������Ϊ___________g��
(5)��������еĴ�ͭ�缫��ΪPt�缫��������ܻ�ѧ����ʽΪ___________________________��
���𰸡�N2H4(l )+O2(g)=N2(g)+2H2O(l) ��H=-624kJ/mol ���� O2+4e-+2H2O=4OH- �� 2Cl--2e-=Cl2�� ʪ��ĵ⻯�ص�����ֽ �� ��ͭ�ľ��� 0.8 2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4
2Cu+O2��+2H2SO4
��������
(1)�����Ȼ�ѧ����ʽ��д��������ע���ʾۼ�״̬�Ͷ�Ӧ���ķ�Ӧ��д���Ȼ�ѧ����ʽ��
(2)�������������õ��ӷ�����ԭ��Ӧ��
(3)��װ����ʯī�缫���Դ�������ӣ�Ϊ�������������������ӷŵ��������������������ķ�������ʪ��ĵ��۵⻯����ֽ���۲��Ƿ���������ݵ���ܷ�Ӧ����ʽ���ж���Һ������ԣ�
(4)����ͬһ�պϻ�·��ת�Ƶ�����ȣ��г���ϵʽ��N2H4��2Cu���з�����⣻
(5)Pt�缫Ϊ���Ե缫���ö��Ե缫���CuSO4��Һ���������ӷŵ���Ⱥ�˳��ȷ����Һ���ܷ�Ӧ����ʽ��
(1)16.0g��̬��(N2H4)���ʵ���Ϊn(N2H4)=16g��32g/mol=0.5mol������������ȫȼ�����ɵ�����ˮ���ų�����312kJ��1mol��̬��(N2H4)ȼ�շ���624kJ����Ӧ���Ȼ�ѧ����ʽΪ��N2H4(l )+O2(g)=N2(g)+2H2O(l) ��H=-624kJ/mol��
(2)��װ����ͨ������ĵ缫Ϊ�����������Ͽ����е������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ��O2+4e-+2H2O=4OH-��
(3)����װ��ͼ��֪����װ����ʯī�缫���Ӽ�װ�õ������������������������������ӷŵ������������缫��ӦʽΪ��2Cl--2e-=Cl2�������������ķ�������ʪ��ĵ��۵⻯����ֽ�����۲쵽ʪ��ĵ��۵⻯����ֽ��������֤������������������Ϊ���Ե缫����ⱥ��ʳ��ˮ���ܷ�Ӧ����ʽΪ��2NaCl+2H2O![]() Cl2��+H2��+2NaOH���ɼ����һ��ʱ����ҳ��е���Һ�ʼ��ԣ�
Cl2��+H2��+2NaOH���ɼ����һ��ʱ����ҳ��е���Һ�ʼ��ԣ�
(4)��װ���д�ͭ���ӵ�Դ������������������ͭ���ӵ�Դ�ĸ������������������Ϊ����ͭ��Һ�����ͼ���ñ�װ��ģ�ҵ�е�ͭ�ľ���ԭ����������ͬһ�պϻ�·�е���ת����Ŀ��ȣ����Ը��ݹ�ϵʽ��N2H4��2Cu��n(Cu)=3.2g��64g/mol=0.05mol������n(N2H4)=![]() n(Cu)=
n(Cu)=![]() ��0.05mol=0.025mol����m(N2H4)= 0.025mol��32g/mol=0.8g��
��0.05mol=0.025mol����m(N2H4)= 0.025mol��32g/mol=0.8g��
(5)��������еĴ�ͭ�缫��ΪPt�缫������Pt�缫Ϊ���Ե缫���������������Һ�е�OH-ʧȥ���ӣ���ΪO2�������ϣ���Һ�е�Cu2+��õ��ӱ�ΪCu���ʣ����Ա����ܻ�ѧ����ʽΪ2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4��
2Cu+O2��+2H2SO4��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�������¸ֹܲ��ܸ�ʴ����ʹ����( )
��ֱ����Դ�������� ��ͭ������
��п������ ��ֱ����Դ��������
A.�٢�B.�ۢ�C.�٢�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ��������Cu��Cu2O��CuO�Ĺ����������ֳ����ȷݡ�����һ��ͨ��������������ַ�Ӧ���������Ϊ25.6g����һ�ݼ���500mLϡ�����й���ǡ����ȫ�ܽⲢ������״���µ�NO����4.48L����֪Cu2O+2H+=Cu+Cu2++H2O����ϡ�����Ũ��Ϊ
A. 4mo1��L-1 B. 2mo1��L-1 C. 1.6mo1��L-1 D. 0.8mo1��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ʫ�ʴ�ᡷ�����������л���ͳ�Ļ������̺������ѧ֪ʶ������ʫ����й�˵���������
A. ����ʯʫ�䡰���糸�����ϣ�ҹ��������ͤ�ޡ���������ʵ���˴����е��Ĺ̶�
B. ��ǫʫ�䡰�俪������ڽ𣬲���������������� �ڽ�ָ����ʯ��
C. �����\ʫ�䡰�ײ��������ɣ����������ƻ������õ��̻���ijЩ����Ԫ�ص���ɫ��Ӧ�й�
D. ������ʫ�䡰ǧ�����������࣬������ɳʼ���𡱡��������ȶ�����������̬�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ϊ�о��绯ѧԭ���������ͼװ�ã�������������ȷ����
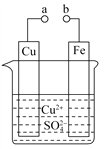
A. a��b������ʱ����Ƭ�ϻ��н���ͭ����
B. a��b�õ�������ʱ����Ƭ�Ϸ����ķ�ӦΪ�� Fe2e===Fe2+
C. a��b�õ�������ʱ�����Ӵ�CuƬ������Ƭ
D. a��b�õ�������ʱ��Cu2+��ͭ�缫�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.ij�¶�ʱ����һ��10L���������У�X��Y��Z��Ϊ���壬�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ��������գ�

��1���÷�Ӧ�Ļ�ѧ����ʽΪ_________________��
��2����Ӧ��ʼ��2min��������X��ʾ��ƽ����Ӧ����Ϊ________________��
��3��ƽ��ʱ�����������ѹǿ����ʼʱ��________________�����������������С�������������ͬ�������������ܶ�����ʼʱ��________________��
��4����amolX��bmolY�Ļ�����巢��������Ӧ����Ӧ��ijʱ�̸����ʵ���ǡ�����㣺n(X)=n(Y)=2n(Z)����ԭ���������a��b=____��
�����ں��º�ѹ���ܱ������У����������������ٷ�������ʱ���ٻ�������ѹǿ���ڻ��������ܶȣ��ۻ������������ʵ������ܻ�������ƽ����Է����������ݸ���Ӧ���������ķ�Ӧ����֮�ȵ��ڻ�ѧ������֮��
��1��һ����֤��2NO2(g)![]() N2O4(g)�ﵽƽ��״̬����________������ţ���ͬ����
N2O4(g)�ﵽƽ��״̬����________������ţ���ͬ����
��2��һ����֤��NH2COONH4(s)![]() CO2(g)+2NH3(g)�ﵽƽ��״̬����______��
CO2(g)+2NH3(g)�ﵽƽ��״̬����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͨ�����з�ɢϵʱ���ܲ��������ЧӦ����
A.������ҺB.ϡ����
C.��ˮD.�����������Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A(g)+ 5B(g)== 4C(g)+ 6D(g)��10L���ܱ������н��У�����Ӻ�D�����ʵ���������0.45mol����˷�Ӧ��ƽ������v(x)�ɱ�ʾΪ( )
A. v(A)=0.0010mol��L-1��s-1
B. v(B)=0.0010mol��L-1��s-1
C. v(C)=0.010mol��L-1��s-1
D. v(D)=0.045mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��E����ѧ������5�ֻ����A��B�����������֮���ת����ϵ����ͼ��ʾ��������˵����ȷ���ǣ� ��

A. X��A��Ӧ�Ļ�ѧ����ʽ�ǣ�Al2O3 + 2Fe ![]() Fe2O3 + 2Al
Fe2O3 + 2Al
B. ����D��Һ�еĽ��������ӵķ�Ӧ��Fe3++3SCN��= Fe(SCN)3��
C. ����Y��һ������������ˮ�����û���Ӧ
D. ���ڻ�����B��C���������ᷴӦ��������Ӧ�����Ծ������Ի�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com