
串联电路中的四个电解池分别装有0.05mol•L﹣1下列溶液,用惰性电极电解,连接直流电源一段时间后,溶液的pH最小的是(假定产生的气体全部放出)()
A. KNO3 B. NaCl C. AgNO3 D. CuCl2
考点: 电解原理.
专题: 电化学专题.
分析: 根据放电顺序确定所得溶液的溶质,根据溶质的酸碱性确定选项.
解答: 解:阳离子的放电顺序为:Ag+>Cu2+>H+>Na+>K+,阴离子的放电顺序为:I﹣>Br﹣>Cl﹣>OH﹣,
根据离子的放电顺序,电解各溶液的电解方程式分别为:
A、电解KNO3溶液实际是电解水,2H2O 2H2↑+O2↑,所得溶液仍是硝酸钾溶液,只是浓度增大,呈中性.
2H2↑+O2↑,所得溶液仍是硝酸钾溶液,只是浓度增大,呈中性.
B、电解NaCl溶液的电解方程式为:2 NaCl+2H2O H2↑+Cl2↑+2NaOH,所得溶液为氢氧化钠溶液,呈碱性;
H2↑+Cl2↑+2NaOH,所得溶液为氢氧化钠溶液,呈碱性;
C、电解Ag NO3溶液的电解方程式为:4AgNO3+2H2O 4Ag+O2↑+4HNO3,所得溶液为硝酸溶液,呈酸性;
4Ag+O2↑+4HNO3,所得溶液为硝酸溶液,呈酸性;
D、电解CuCl2溶液的电解方程式为:CuCl2 Cu+Cl2↑,所得液体为水;
Cu+Cl2↑,所得液体为水;
故选C.
点评: 本题考查了电解原理,知道阴阳离子的放电顺序解本题的关键;电解电解质溶液时,电解类型有:电解水型、电解电解质型、电解电解质和水型,题目难度中等.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. 无色溶液中:K+、H+、Fe2+、NO3﹣
无色溶液中:K+、H+、Fe2+、NO3﹣
B. c(H+)<c(OH﹣)的溶液中:Na+、K+、SO42﹣、ClO﹣
C. 含0.1mol•L﹣1 HCO3﹣的溶液中:Al3+、Ca2+、NO3﹣、SO42﹣
D. 含0.1 mol•L﹣1 SCN﹣的溶液中:Fe3+、NH4+、NO3﹣、Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为:
H2(g)+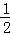 O2(g)=H2O(l)△H=﹣285.8kJ/mol
O2(g)=H2O(l)△H=﹣285.8kJ/mol
CO(g)+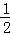 O2(g)=CO2(g)△H=﹣282.6kJ/mol
O2(g)=CO2(g)△H=﹣282.6kJ/mol
C8H18(l)+ O2(g)=8CO2(g)+9H2O(l)△H=﹣5472kJ/mol
O2(g)=8CO2(g)+9H2O(l)△H=﹣5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=﹣889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是()
A. H2(g) B. CO(g) C. C8H18(l) D. CH4(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液电解一段时间后,再加入相关物质,溶液能恢复原状况的是()
电解质溶液 阳极 阴极 加入的物质
A NaCl溶液 碳 铁 盐酸
B NaOH溶液 碳 碳 水
C 硫酸铜溶液 铜 碳 硫酸铜
D 硫酸 铁 碳 H2O
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
A. AgNO3 B. Na2SO4 C. CuCl2 D. KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐与碱反应制得白色纯净的Fe(OH)2沉淀.某研究性小组在研究制备Fe(OH)2的过程中,按图进行实验,最终在两极间的溶液中首先观察到白色沉淀.

(1)请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水②NaCl溶液③NaOH溶液④四氯化碳⑤CuCl2溶液⑥乙醇⑦铁棒⑧植物油⑨碳棒
a为 ,b为 ,c为 ,d为 .(填序号)
(2)书写电极反应式:
阳极 ;.阴极 .
(3)c的作用是 .
(4)在加入c之前,对d溶液的简单处理应是 ,这样处理的目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
鼠尾草酚用于防治骨质疏松,鼠尾草酸可两步转化得到鼠尾草酚,下列说法正确的是
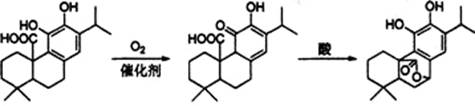
X(鼠尾草酸) Y(鼠尾草酸酮) Z(鼠尾草酚)
A. X、Y、Z属于芳香族化合物
B. X、Y、Z均能与FeCl3溶液发生显色反应
C. 1 mol X或1 mol Z与NaOH溶液反应,均最多消耗3 mol NaOH
D. X、Y、Z均能与溴的四氯化碳溶液发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:
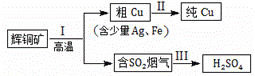
(1) Cu2S中Cu元素的化合价是 价。
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
① 粗铜应与直流电源的 极(填“正”或“负”)相连。
② 铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是 。
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。
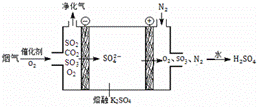
① 在阴极放电的物质是 。
② 在阳极生成SO3的电极反应式是 。
(4)检测烟气中SO2脱除率的步骤如下:
i.将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
ii.加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
iii.过滤、洗涤、干燥,称量沉淀质量。
① 用离子方程式表示i中溴水的主要作用 。
② 若沉淀的质量越大,说明SO2的脱除率越 (填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com