
【题目】磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)H3PO2是一元中强酸,写出其电离方程式:_______;请将NaH2PO2溶液中的各离子按浓度由大到小的顺序排列:__________。
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是_______,其原因是__________。
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是_______(填化学式)。
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式________,若反应中转移电子6NA,用去还原剂_____mol。再向Ba(H2PO2)2溶液中加入盐酸制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:_______。
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:_______。
【答案】H3PO2![]() H++ H2PO2- Na+、H2PO2-、OH-、H+ Na2CO3 H3PO2是中强酸,碳酸是弱酸,CO32–的水解程度大于H2PO2- H3PO4 2P4+ 3Ba(OH)2+ 6H2O →2PH3↑+ Ba(H2PO2)2 1.5mol 用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物H3PO2分离(合理即得分) 阳极反应中消耗水电离的OH—,使c(H+)增大,H2PO2-通过阴离子交换膜进入阳极室,得到产品
H++ H2PO2- Na+、H2PO2-、OH-、H+ Na2CO3 H3PO2是中强酸,碳酸是弱酸,CO32–的水解程度大于H2PO2- H3PO4 2P4+ 3Ba(OH)2+ 6H2O →2PH3↑+ Ba(H2PO2)2 1.5mol 用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物H3PO2分离(合理即得分) 阳极反应中消耗水电离的OH—,使c(H+)增大,H2PO2-通过阴离子交换膜进入阳极室,得到产品
【解析】
![]() 根据
根据![]() 是一元中强酸可知,
是一元中强酸可知,![]() 是弱电解质,溶液中部分电离出氢离子,据此写出电离方程式;根据
是弱电解质,溶液中部分电离出氢离子,据此写出电离方程式;根据![]() 是一元中强酸,可以判断
是一元中强酸,可以判断![]() 为正盐,是强碱弱酸盐,水解显碱性;
为正盐,是强碱弱酸盐,水解显碱性;![]() 是一元中强酸,碳酸是弱酸,酸性越弱其对应盐的水解程度越大;
是一元中强酸,碳酸是弱酸,酸性越弱其对应盐的水解程度越大;![]() 和
和![]() 溶液反应进行化学镀银,此反应中氧化剂与还原剂的物质的量之比为4:1,结合化合价判断产物;
溶液反应进行化学镀银,此反应中氧化剂与还原剂的物质的量之比为4:1,结合化合价判断产物;![]() 根据反应物和生成物结合原子守恒和电子守恒书写方程式;
根据反应物和生成物结合原子守恒和电子守恒书写方程式;![]() 阳极反应中消耗水电离的
阳极反应中消耗水电离的![]() ,使
,使![]() 增大,
增大,![]() 通过阴离子交换膜进入阳极室,得到产品。
通过阴离子交换膜进入阳极室,得到产品。
![]() 是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为
是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为![]() ;由于
;由于![]() 是一元中强酸,所以
是一元中强酸,所以![]() 为一元强碱和一元中强酸形成的正盐,所以该盐溶液由于
为一元强碱和一元中强酸形成的正盐,所以该盐溶液由于![]() 发生水解成碱性,方程式为
发生水解成碱性,方程式为![]() ,所以溶液中离子浓度由大到小的顺序为
,所以溶液中离子浓度由大到小的顺序为![]() ;故答案为:
;故答案为:![]() ;
;![]() 是一元中强酸,碳酸是弱酸,酸性越弱其对应盐的水解程度越大,所以相同物质的量浓度的
是一元中强酸,碳酸是弱酸,酸性越弱其对应盐的水解程度越大,所以相同物质的量浓度的![]() 溶液的碱性比
溶液的碱性比![]() 溶液强,故答案为:
溶液强,故答案为:![]() ;
;![]() 是中强酸,碳酸是弱酸,
是中强酸,碳酸是弱酸,![]() 的水解程度大于
的水解程度大于![]() ;
;![]() 该反应中
该反应中![]() 为氧化剂,
为氧化剂,![]() 为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,
为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,![]() ,解得
,解得![]() ,所以氧化产物为
,所以氧化产物为![]() 价的
价的![]() ,故答案为:
,故答案为:![]() ;
;![]() 白磷
白磷![]() 与
与![]() 溶液反应生成
溶液反应生成![]() 气体和
气体和![]() ,反应方程式为
,反应方程式为![]() ,每生成
,每生成![]() 有6molP被氧化,即
有6molP被氧化,即![]() 被氧化,转移电子6mol;用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物
被氧化,转移电子6mol;用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物![]() 分离,故答案为:
分离,故答案为:![]() ;
;![]() ;用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物
;用硫酸代替盐酸生成的硫酸钡是沉淀,易于与产物![]() 分离;
分离;![]() 据电解反应式可知,阳极反应中消耗水电离的
据电解反应式可知,阳极反应中消耗水电离的![]() ,使
,使![]() 增大,
增大,![]() 通过阴离子交换膜进入阳极室,得到产品,故答案为:阳极反应中消耗水电离的
通过阴离子交换膜进入阳极室,得到产品,故答案为:阳极反应中消耗水电离的![]() ,使
,使![]() 增大,
增大,![]() 通过阴离子交换膜进入阳极室,得到产品。
通过阴离子交换膜进入阳极室,得到产品。


科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)+Q1 K1 (Ⅰ)
2NO(g)+Cl2(g)2ClNO(g)+Q2 K2 (Ⅱ)
(1)4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用含K1、K2的代数式表示).
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡.测得在10min内v(ClNO)=7.5×10﹣3molL﹣1min﹣1,则平衡后n(Cl2)=_____mol,NO的转化率а1=____.其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率а2____а1(填“>”“<”或“=”),平衡常数K2____(填“增大”“减小”或“不变”).若要使K2减小,可采用的措施是____.
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH→NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1的CH3COONa溶液,则两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为____.(已知HNO2的电离常数Ka=7.1×10﹣4molL﹣1,CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1,可使溶液A和溶液B的pH相等的方法是____.
a 向溶液A中加适量水 b 向溶液A中加适量NaOH
c 向溶液B中加适量水 d 溶液B中加适量NaOH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列关于焓变的说法正确的是( )
A.相同条件下反应2SO2(g)+O2(g)![]() 2SO3(g)与4SO2(g)+2O2(g)
2SO3(g)与4SO2(g)+2O2(g)![]() 4SO3(g)的△H相等
4SO3(g)的△H相等
B.甲烷的标准燃烧热为-890.3kJ/mol,则甲烷燃烧的热化学方程式可以表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
C.在一定温度和压强下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
D.一定条件2SO2(g)+O2(g)![]() 2SO3(g) △H1,2SO2(g)+O2(g)
2SO3(g) △H1,2SO2(g)+O2(g)![]() 2SO3(l) △H2,则△H1>△H2
2SO3(l) △H2,则△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是将_____能转化成_____能的一种装置。一种利用原电池原理制备NH3的装置如图所示,陶瓷在高温时可以传输H+。该设备中,电极____(填“a”或“b”)作负极,其电极反应式为:_____。当电路中通过1.2mol的电子时,可生成NH3____mol。
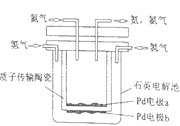
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定不能大量共存的是
A.使淀粉碘化钾试纸变蓝的溶液中:K+、SO42-、Na+、ClO-
B.使石蕊试液变红的溶液中:Al3+、Cl-、NH4+、NO3-
C.c(Al3+) = 0.1 mol/L的溶液中:AlO2-、Na+、Cl-、K+
D.![]() = 1×10-13 的溶液中:CH3COO-、CO32-、K+、SO32-
= 1×10-13 的溶液中:CH3COO-、CO32-、K+、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醛类是香料中重要的一族,铃兰醛具有令人愉快的香味。以下是合称铃兰醛的一种路线:
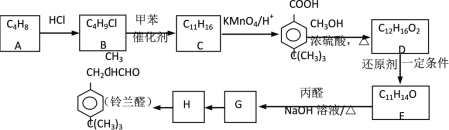
已知:① R1―CHO + R2―CH2―CHO ![]() R1―CH=C―CHO
R1―CH=C―CHO
② R―Cl +![]()
![]()
![]() + HCl
+ HCl
完成下列填空:
(1)写出A的名称_____________。
(2)写出结构简式:C_______;E_________。
(3)化合物M是G的芳香族同分异构体,M符合以下条件:
①能发生银镜反应;②在苯环的1,3,5位有三个侧链,其中两个烃基是C2H3和C4H9,则符合条件M的同分异构体共_______种。
(4)写出H生成铃兰醛的化学方程式:_______。
(5)E向G转化的过程中,常有分子式为C17H22O的副产物K产生。K的结构简式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种物质的转化关系。下列组合中不符合该关系的是( )
X | Y | Z | W |
| |
A | Na2CO3 | CO2 | CaCO3 | Ca(HCO3)2 | |
B | SO2 | Na2SO3 | H2SO4 | NaHSO3 | |
C | HCl | FeCl2 | Cl2 | FeCl3 | |
D | Na2O2 | NaOH | Na2CO3 | NaHCO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是环境污染物,研究氮氧化物转化有重要的意义。回答下列问题:
(1)催化转化器可使汽车尾气反应而转化:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH
已知:2C(s)+O2(g)=2CO(g) ΔH1=akJ·mol-1;
C(s)+O2(g)=CO2(g) ΔH2=bkJ·mol-1;
N2(g)+O2(g)=2NO(g) ΔH3=ckJ·mol-1
ΔH=__kJ·mol-1(用含a、b、c的代数式表示);
(2)T℃时,将等物质的量的NO和CO充入容积为1L的密闭容器中发生尾气转化反应,容器中NO物质的量随时间变化如图所示。
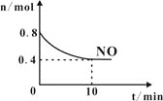
①T℃时,该化学反应的平衡常数K=___。
②下列事实能判断汽车尾气转化反应达到到化学平衡状态的是___;
A.体系中NO的转化率和CO的转化率相等 B.气体的密度不再变化
C.NO消耗速率等于N2消耗速率的2倍 D.混合气体平均相对分子质量不再变化
③已知汽车尾气转化反应的ΔH<0。10min后,改变下列示意图横坐标对应的反应条件,纵坐标对应的量变化关系不正确的是___。(填序号)
a.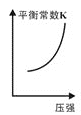 b.
b.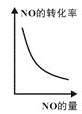 c.
c.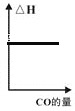 d.
d.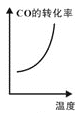
(3)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)![]() 2I(g)(快反应)
2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
下列表述不正确的是___(填标号)。
A.IO为反应的中间产物
B.第二步活化能比第三步小
C.第二步对总反应速率起决定作用
D.N2O分解反应中,k值与是否含碘蒸气无关
(4)碱吸收、碳还原是目前工业生产中处理氮氧化物的常用方法。
①碱吸收的常见产物为NaNO2。常温下,pH=8的NaNO2溶液中c(Na+)-c(NO2-)=___mol·L-1(用精确值表示);
②碳还原法是在高温条件下将NO与NO2混合气体与焦炭反应,生成CO2和N2,且物质的量之比为4:3,写出该方法的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO和H2在Co做催化剂、温度为160℃~200℃时,可以合成汽油(即分子中含5至8个碳原子的烷烃).
(1)用CnH2n+2表示汽油,写出上述反应的化学方程式_______(需配平)
(2)若向密闭的合成塔内通入CO和H2,恰好完全反应,此时塔内压强降至反应前的![]() ,通过计算说明是否生成汽油______________________.
,通过计算说明是否生成汽油______________________.
(3)以天然气、焦炭、水为初始原料,可以制得CO和H2,进而人工合成汽油.(流程示意图如下,反应③的H2也由反应①得到.)
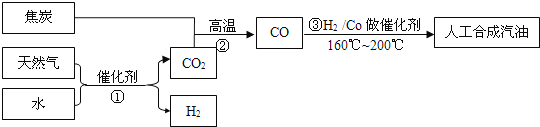
若反应①、②、③的转化率均为100%,且将反应①中得到的CO2和H2全部用于合成人工汽油.
(a)通过计算说明上述方案能否得到理想的产品________________.
(b)当CO2的使用量应控制为反应①中CO2产量的_____(填比例范围),可以得到理想的产品.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com