
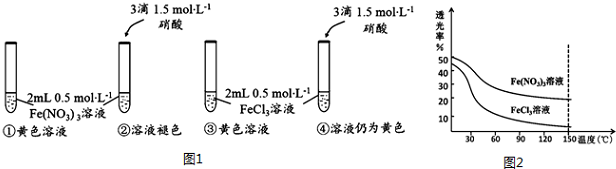
分析 (1)实验①②对比,硝酸铁溶液加入硝酸溶液,溶液中氢离子浓度增大,而溶液黄色褪去,信息①中平衡向左移动,硝酸铁溶液溶液黄色是[Fe(H2O)6-n(OH)n]3-n所致;
(2)实验②④对比,氯化铁溶液中加入硝酸,溶液黄色不变,氯化铁溶液黄色为[FeCl4(H2O)2]-所致;
(3)随着温度升高,Fe(NO3)3溶液透光率逐渐减小,说明溶液中[Fe(H2O)6-n(OH)n]3-n浓度增大;
(4)升高温度溶液中[FeCl4(H2O)2]-浓度增大;
(5)加入含有氯离子物质,由平衡移动增大溶液中[FeCl4(H2O)2]-浓度.
解答 解:(1)实验①②对比,硝酸铁溶液加入硝酸溶液,溶液中氢离子浓度增大,而溶液黄色褪去,信息①中平衡向左移动,硝酸铁溶液溶液黄色是[Fe(H2O)6]3+水解产生了[Fe(H2O)6-n(OH)n]3-n所致,
故答案为:[Fe(H2O)6]3+水解产生了[Fe(H2O)6-n(OH)n]3-n;
(2)试管②、④中加入等量的HNO3后,②中溶液褪色,而④中溶液仍呈黄色,说明氯化铁溶液黄色为[FeCl4(H2O)2]-所致,
故答案为:[FeCl4(H2O)2]-; 试管②、④中加入等量的HNO3后,②中溶液褪色,而④中溶液仍呈黄色;
(3)温度升高,导致平衡[Fe(H2O)6]3++nH2O?[Fe(H2O)6-n(OH)n]3-n+nH3O+正向移动,[Fe(H2O)6-n(OH)n]3-n浓度增大,溶液颜色加深,Fe(NO3)3溶液透光率逐渐减小,
故答案为:温度升高,导致平衡[Fe(H2O)6]3++nH2O?[Fe(H2O)6-n(OH)n]3-n+nH3O+正向移动,[Fe(H2O)6-n(OH)n]3-n浓度增大,溶液颜色加深;
(4)升高温度溶液中[FeCl4(H2O)2]-浓度增大,促进[Fe(H2O)6]3++4Cl-?[FeCl4(H2O)2]-+4H2O 正向进行,正反应为吸热反应,
故答案为:[Fe(H2O)6]3++4Cl-?[FeCl4(H2O)2]-+4H2O;吸热;
(5)对照实验②④可知,向②的溶液中加入含有氯离子物质,增大溶液中[FeCl4(H2O)2]-浓度,可以证明实验方案验证(4)中结论,由于D中氯化铁溶液本身含有[FeCl4(H2O)2]-,不能选用,
故答案为:B.
点评 本题考查了对探究实验方案分析评价、信息获取与迁移运用,注意充分利用对照实验进行分析,是对现实综合能力的考查,难度较大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子数相同 | B. | 中子数相同 | C. | 质子数相同 | D. | 气体质量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该有机物的化学式为C12H12O6 | |
| B. | 1mol该有机物最多可以和3molNaOH反应 | |
| C. | 该有机物容易发生加成、取代、消去等反应 | |
| D. | 该有机物可代替KSCN检验Fe3的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
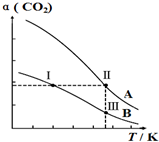 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )| A. | 反应2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g)的△S<0、△H<0 | |
| B. | 表示乙容器CO2的平衡转化率随温度变化的是曲线B | |
| C. | 体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ) | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
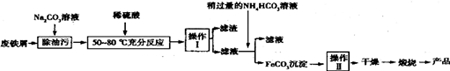
 HCO3-+OH-;
HCO3-+OH-;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去乙烷中少量的乙烯:与氢气混合加热,把乙烯转化为乙烷 | |
| B. | 除去苯中的少量乙烯:加入浓溴水振荡静置后过滤,除去二溴乙烯 | |
| C. | 为加快反应速率,制乙炔时用食盐水代替水 | |
| D. | 提取碘水中的碘,加入CCl4振荡静置分层后,取出有机层再分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:9 | B. | 9:1 | C. | 1:11 | D. | 11:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com