
在下列有关晶体的叙述错误的是
A.离子晶体中,一定存在离子键 B.原子晶体中,只存在共价键
C.离子晶体中可能存在共价键 D.分子晶体中有可能存在离子键
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
下列七种晶体:A.二氧化硅 B.乙烷 C.碳酸钠 D.晶体硅 E.氩气
F.过氧化氢 G.镁 H.氢气(用字母填空)
(1)属于原子晶体的是__________,不存在任何化学键的是 ;
(2)只含有非极性键的物质是____________,既有极性键又有非极性键的物质是 ,含有离子键、共价键的化合物是___________;
(3)在一定条件下能导电且导电时未发生化学反应的单质是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )

A.原混合酸中NO3-物质的量浓度为2 mol/L
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D. H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中肯定错误的是
A.某原子K层上只有一个电子
B.某原子M层上电子数为L层电子数的4倍
C.某离子M层上和L层上的电子数均为K层的4倍
D.阳离子的最外层电子数可能为2,也可能为8
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C原子序数依次递增,它们原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是
A.原子半径A<B<C B.A的氢化物的稳定性大于C的氢化物的稳定性
C.C的氧化物的熔点比A的氧化物的低 D.A与C可形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氢化锂(LiH)属于离子化合物,LiH跟水反应可以反出氢气。下列叙述正确的是
A.LiH跟水反应时的水溶液显中性 B.LiH中氢离子可以被还原成氢气
C.LiH在化学反应中是一种强氧化剂 D.LiH中氢离子半径比锂离子半径大
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃以任意比例混合,在150℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,下列各组混合烃中不符合此条件的是( )
A. CH4 C2H4 B. CH4 C3H6 C. C2H4 C3H4 D. CH4 C3H4
查看答案和解析>>
科目:高中化学 来源: 题型:
在氯化铁溶液中存在下列平衡:FeCl3+3H2O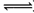 Fe(OH)3+3HC1;△H>0。回答下列问题:
Fe(OH)3+3HC1;△H>0。回答下列问题:
(1)加热FeCl3溶液,溶液的颜色会不断加深,可得到一种红褐色透明液体,向这种液
体中加入MgCl2溶液,产生的现象为 。
(2)不断加热FeCl3溶液,蒸干其水分并灼烧得到的固体可能是 。
(3)在配制FeCl3溶液时,为防止浑浊,应加入 。
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤
后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH小于4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;
若pH<7,则H2A是强酸
C.用0.200 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的
浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度: ④>①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com