
����Ŀ����2 L�ĺ����ܱ������г���A(g)��B(g)��������ӦA(g)+B(g)![]() 2C(g)+D(s) ��H=a kJ��mol��1��ʵ�����ݺͽ���ֱ������ͼ��ʾ������˵������ȷ����
2C(g)+D(s) ��H=a kJ��mol��1��ʵ�����ݺͽ���ֱ������ͼ��ʾ������˵������ȷ����
ʵ����� | �¶� | ��ʼ���ʵ��� | �����仯 | |
A | B | |||
I | 600�� | 1mol | 3mol | 96kJ |
II | 800�� | 1.5mol | 0.5mol | ���� |
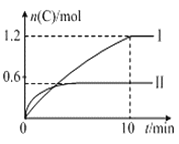
A. ʵ����У�10 min��ƽ������v(B)��0.03 mol��L��1��min��1
B. ��������ʽ��a��160
C. 600 ��ʱ���÷�Ӧ��ƽ�ⳣ����1.5
D. ��ʵ����ƽ����ϵ���ٳ���0.5 mol A��1.5 mol B��A��ת��������
���𰸡�B
��������
A.ʵ����У�10 min������C�����ʵ�����1.2mol������ݷ���ʽ��֪����BΪ0.6mol��Ũ�ȼ�С0.3mol/L����ƽ������v��B��=0.3mol/L��10min=0.03 mol��L��1��min��1����A˵����ȷ��
B.��ʵ����֪������1.2molC�����仯Ϊ96KJ��������2molC�������仯Ϊ![]() ��2=160KJ������ʽ��a=-160����B˵������
��2=160KJ������ʽ��a=-160����B˵������
C.������ͼ��֪��ʵ�����600C������10minʱ�ﵽƽ��״̬����ʱA��B��C�����ʵ����ֱ�Ϊ:0.4mol��2.4mol��1.2mol��Ũ��Ϊ0.2mol/L��1.2mol/L��0.6mol/L��ƽ�ⳣ��K=![]() =1.5����C˵����ȷ��
=1.5����C˵����ȷ��
D.��ʵ����ƽ����ϵ���ٳ���0.5 mol A��1.5 mol B����A��B����ʼ���ʵ���֮����3:1��Ϊ3:3���൱������B��Ũ�ȣ�A��ת��������D˵����ȷ��
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)����(![]() )��С�մ�(
)��С�մ�(![]() )�㷺Ӧ����ʳƷ�ӹ����մ����ԭ���к���С�մ��ں決���ȹ��̣�С�մ����ֽⷴӦ���÷�Ӧ�Ļ�ѧ����ʽ��______���մ���ɿ����ʵ���������θ��(��Ҫ�ɷ�����)����֢״���÷�Ӧ�Ļ�ѧ����ʽ��_______��
)�㷺Ӧ����ʳƷ�ӹ����մ����ԭ���к���С�մ��ں決���ȹ��̣�С�մ����ֽⷴӦ���÷�Ӧ�Ļ�ѧ����ʽ��______���մ���ɿ����ʵ���������θ��(��Ҫ�ɷ�����)����֢״���÷�Ӧ�Ļ�ѧ����ʽ��_______��

(2)ijͬѧ������ͼװ��(�г���������ȥ)�о������С�մ�����ʡ�
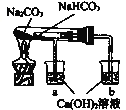
�ٸ�ʵ���Ŀ����_______��
�ڹ۲쵽�а�ɫ�������ɵ��ձ���_________(����ĸ���)��
��ʵ�������__________��
��Ϊ��һ�������о�̼�����Ƶ����ʣ���ͬѧ����ƽȷ����![]() ̼�����ƣ���������Ϊ
̼�����ƣ���������Ϊ![]() �������м��ȣ���ȴ������������������ʣ������������Ϊ______
�������м��ȣ���ȴ������������������ʣ������������Ϊ______![]() ����ʵ�ʳƵõ������ȸ���ֵҪ���ܵ�ԭ����________���Ľ��IJ���������_______________��
����ʵ�ʳƵõ������ȸ���ֵҪ���ܵ�ԭ����________���Ľ��IJ���������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з������з�ӦaA(g) ![]() cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����
A. A��ת���ʱ��
B. ƽ��������Ӧ�����ƶ�
C. D������������
D. a < c��d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��װ�ý��е���Ӧʵ�飬���ܴﵽʵ��Ŀ�ĵ���
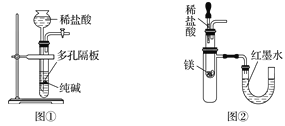
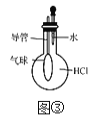
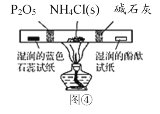
A. ��ͼ����ʾװ����ȡ����������CO2����
B. ��ͼ����ʾװ����֤þ�����ᷴӦ����ЧӦ
C. ��ͼ����ʾװ����֤HCl����������ˮ
D. ��ͼ����ʾװ�ü���NH4Cl�ֽ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ����ȷ����(����)
A. �����ȼ������H����890.3 kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ CH4(g)��2O2(g)===CO2(g)��2H2O(g)����H����890.3 kJ��mol��1
B. 500 �桢30 MPa������0.5 mol N2(g)��1.5 mol H2(g)�����ܱ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪN2(g)��3H2(g)![]() 2NH3(g)����H����38.6 kJ��mol��1
2NH3(g)����H����38.6 kJ��mol��1
C. HCl��NaOH��Ӧ���к�����H����57.3 kJ��mol��1����H2SO4��Ca(OH)2��Ӧ���к�����H��2��(��57.3)kJ��mol��1
D. ��101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ2H2(g)��O2(g)===2H2O(l)����H����571.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������˵����ȷ����( )
A. ��0.1 mol Na2O2�ľ�����������������������Ϊ0.4NA
B. 46 g NO2��N2O4�Ļ�������к��е���ԭ����Ϊ2NA
C. 1 mol Fe��һ��������ǡ����ȫ��Ӧʱ��ת�Ƶ�����һ��Ϊ3NA
D. 1 mol CH4�������������ȡ����Ӧ������CH3Cl��������ԼΪ22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݵȵ���ԭ���жϣ�����˵���д������(����)
A. B3N3H6������ģ����ͼ������������ԭ�Ӿ���ͬһƽ����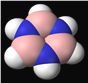
B. B3N3H6�����д���˫�����ɷ����ӳɷ�Ӧ
C. H3O����NH3�ǵȵ����壬��Ϊ������
D. CH4��NH4+�ǵȵ����壬��Ϊ��������ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�������һ������ָ����Һ�д����������
A. ��ʹpH��ֽ����ɫ����Һ�У�Na+��ClO����Fe3+��SO42��
B. ���д���Al3+����Һ�У�K+��Mg2+��NO3����HCO3��
C. ![]() ��1��10��13mol��L��1����Һ�У�NH4����Ca2����Cl����NO3��
��1��10��13mol��L��1����Һ�У�NH4����Ca2����Cl����NO3��
D. ��������ˮ�������c(H+)=10-13 mol��L��1����Һ�У�Na+��Ba2+��HCO3����Cl��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com