
| A. | 配平后的离子方程式为2O3+2I-+4H+=I2+2O2+2H2O | |
| B. | 每生成1 mol I2转移电子2 mol | |
| C. | O2是还原产物之一 | |
| D. | 该反应能说明O2的氧化性大于I2的 |
分析 A、方程式电荷不守恒,电子转移不守恒.根据电子转移守恒、电荷守恒、原子守恒配平;
B、根据方程式结合电子转移情况进行回答
C、氧化剂通过还原反应生成的物质是还原产物,氧气和臭氧中氧元素的化合价相同为0价;
D、根据反应方程式进行的氧化剂大小比较是指氧化剂与氧化产物之间的比较.
解答 解:A、选项中离子方程式电荷不守恒,电子转移不守恒,配平后的方程式为O3+2I-+2H+=I2+O2+H2O,故A错误;
B、反应中氧气和臭氧中氧元素的化合价相同为0价,氧元素化合价由O3中0价降低为H2O中-2价,配平后的方程式为:O3+2I-+2H+=I2+O2+H2O,每生成1 mol I2转移电子2 mol,故B正确;
C、反应中氧气和臭氧中氧元素的化合价相同为0价,氧气不是还原产物,氧元素化合价由O3中0价降低为H2O中-2价,还原产物是H2O,故C错误;
D、根据反应方程式进行的氧化剂大小比较是指氧化剂与氧化产物之间的比较,在该反应中不能比较二者的氧化性强弱,故D错误;
故选:B.
点评 本题考查氧化还原反应的基本概念与计算,难度不大,注意A根据化合价判断氧气不是氧化产物,容易马虎出错,A选项解答利用守恒进行判断即可,不需配平.


科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
. 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2 NA | |
| B. | 2.4g镁离子所含电子数目为NA | |
| C. | 足量铜与1L2mol•L-1稀硫酸反应可以生成H2分子总数为2NA | |
| D. | 标准状况下,44.8 L CCl4中含2NA个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含H+的溶液 | B. | c(H+)=1×10-7mol•L-1 | ||
| C. | pH<7的溶液 | D. | c(OH-)<c(H+)的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:11 | B. | 11:1 | C. | 7:11 | D. | 11:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
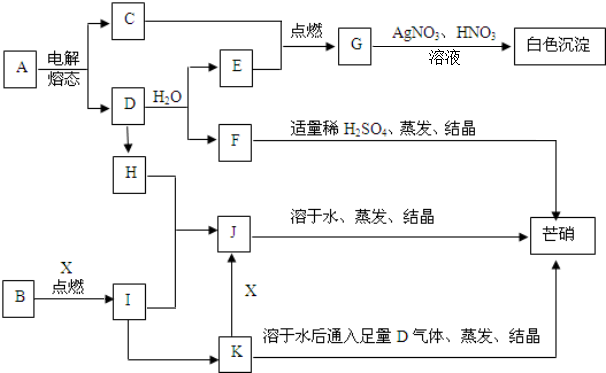
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进行焰色反应时,必须用稀硫酸洗涤并灼烧铂丝,然后再进行实验 | |
| B. | 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 | |
| C. | 读取滴定管内液体体积时,俯视读数导致读数偏小 | |
| D. | 利用一束强光照射明矾水溶液,产生光亮的“通路”,说明明矾一定发生了水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中化学计量数表示分子个数 | |
| B. | 该反应的△H2=+483.6kJ/mol | |
| C. | △H2<△H1 | |
| D. | △H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol•L-1,则反应的△H<0 | |
| B. | 若在2 L恒容绝热(与外界无热量交换)密闭容器中进行该反应,化学平衡常数不变 | |
| C. | 保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO, 反应达到平衡前的速率:v(正)<v(逆) | |
| D. | 保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com